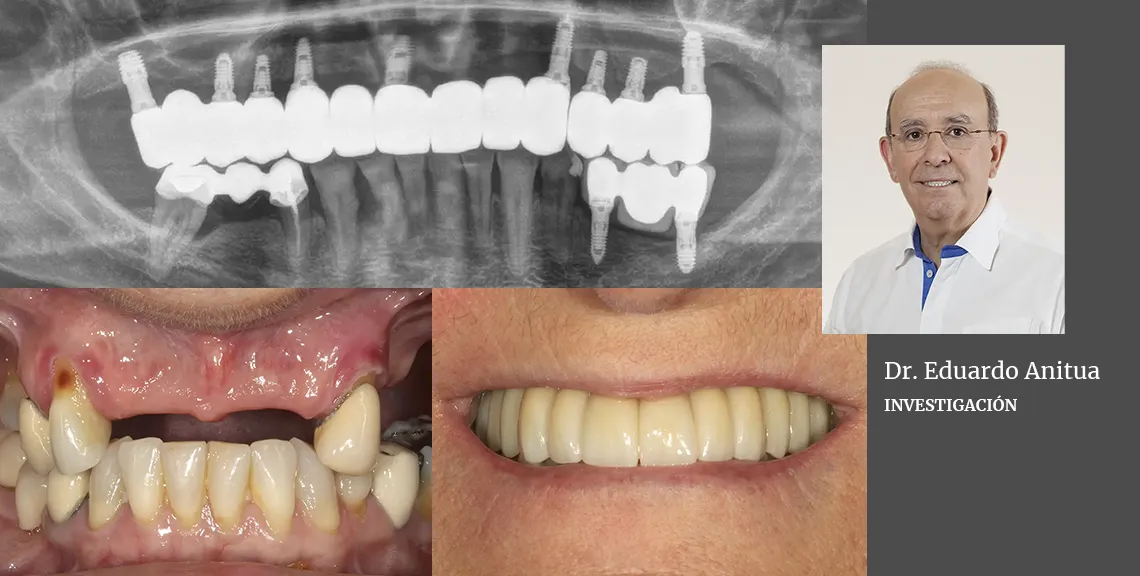
Atrofia extrema del maxilar superior rehabilitada con implantes estrechos y cortos unida al empleo de diferentes técnicas quirúrgicas y protésicas

Dr. Eduardo Anitua
DDS, MD, PhD
Práctica privada en implantología oral, Eduardo Anitua Institute, Vitoria.
Investigador clínico, Eduardo Anitua Foundation, Vitoria.
University Institute for Regenerative Medicine and Oral Implantology – UIRMI (UPV/EHU-Fundación Eduardo Anitua), Vitoria.
Introducción
La utilización de implantes dentales de dimensiones reducidas, tanto en diámetro (implantes estrechos) como en longitud (implantes cortos o extracortos)1,2 se ha consolidado en la práctica clínica de la implantología convencional. Esta tendencia responde, en buena medida, al objetivo de evitar intervenciones quirúrgicas extensas de reconstrucción ósea que, en pacientes con atrofias maxilares o mandibulares importantes, implican una mayor morbilidad, prolongación del tratamiento, incremento de costes y un mayor riesgo de complicaciones3–8. Los defectos de la cresta alveolar tras pérdida dental suelen incluir tanto una reducción vertical como horizontal del hueso, lo que tradicionalmente se abordaba mediante técnicas como elevación de seno maxilar lateral, injertos de bloque, regeneración ósea guiada o distracción osteogénica9–17. Sin embargo, distintas revisiones sistemáticas y meta-análisis han demostrado que los implantes de diámetro reducido y los implantes de longitud reducida alcanzan tasas de éxito y supervivencia comparables a los implantes estándar, siempre que se consideren adecuadamente los factores anatómicos, biomecánicos y de diseño18–21. Por ejemplo, en una revisión sistemática sobre implantes estrechos se reportó que para diámetros de 3,3 a 3,5 mm las tasas de supervivencia se encontraban entre 88,9% y 100%, y las tasas de éxito entre 91,4% y 97,6%22. De hecho, el análisis mostró que no hubo diferencia estadísticamente significativa en supervivencia frente a implantes convencionales (odds ratio = 1.16; IC 0.7-1.69). Otra revisión más reciente indicó tasas medias de supervivencia para implantes estrechos de 94,7 % (categoría < 3 mm), 97,3 % (3,00-3,25 mm) y 97,7 % (3,30-3,50 mm)23. En lo que respecta a los implantes cortos, una revisión reportó una tasa de supervivencia acumulada del 99,1 % (IC 95%; CI: 98.8-99.4) para implantes definidos como “cortos”, con una tasa de éxito biológica de 98,8% (IC 95 %; CI: 97.8-99.8)7. En otro estudio más actual se encontró para implantes de ≤ 6 mm de longitud una supervivencia media del 96% (rango 86,7%-100%) frente al 98% (rango 95%-100%) para implantes de mayor longitud, en periodos de 1 a 5 años. También se ha reportado una tasa de supervivencia del 97% para implantes estrechos tras ~36 meses, con pérdida marginal de hueso de 0,821 mm como media6.
La ventaja principal de esta filosofía es que permite, en muchos casos, resolver rehabilitaciones completas o parciales con intervenciones menos invasivas. Es decir: los implantes estrechos y/o cortos pueden utilizarse de forma aislada o combinada con otras técnicas quirúrgicas mínimamente agresivas, de modo que se puede afrontar una gran atrofia maxilar o mandibular con un abordaje quirúrgico reducido, menor tiempo de tratamiento y menor impacto para el paciente24. Desde el punto de vista clínico-quirúrgico, esta estrategia permite simplificar el protocolo: al disponer de implantes de menor diámetro y/o longitud se reduce la necesidad de injertos (verticales y horizontales), se preserva mayor cantidad de hueso nativo (lo que es especialmente importante en casos de atrofia severa donde el volumen óseo remanente es ya limitado) y se reduce la morbilidad del paciente (menos cirugía, menor tiempo operatorio, menos sangrado, menor postoperatorio)9,25,26. Esta estrategia coincide con la tendencia actual de la “implantología mínimamente invasiva”, que promueve técnicas con menor traumatismo, preservación de los tejidos blandos y óseos, menor tiempo de recuperación y mejores resultados funcionales y estéticos22–24,27–32.Cuando el hueso es escaso, es clave garantizar tanto que haya suficiente volumen óseo remanente con adecuado aporte sanguíneo, como conservar tejido para posibles intervenciones futuras20,21,32–34. En este sentido, los implantes de dimensiones reducidas ofrecen una opción conservadora que, sin comprometer la funcionalidad a largo plazo, permiten no “agotar” el hueso disponible desde la intervención inicial agresiva25,27,29,35–38. Por último, esta filosofía viene acompañada de ventajas prostodóncicas y de secuencia de fresado/implante: usar un mismo tipo de implante (por ejemplo un sistema estrecho o corto) para toda la rehabilitación facilita la logística, reduce los pasos quirúrgicos, simplifica la plataforma protésica y puede favorecer la estandarización del protocolo clínico39. Este enfoque es compatible con la demanda creciente de tratamientos menos complejos para el profesional y de menor carga para los pacientes, sin comprometer los resultados a medio y largo plazo. El camino de la implantología dental se dirige claramente hacia este tipo de actuaciones: intervenciones menos invasivas, preservación ósea, reducción de morbilidad y mantenimiento de altas tasas de éxito. Los datos científicos actuales avalan que los implantes estrechos, cortos y extracortos constituyen una alternativa predecible y eficiente, siempre que se realice una selección adecuada del caso, para la rehabilitación de crestas con atrofia ósea evitando así el recurso sistemático a cirugías de reconstrucción extensiva6,18,40–43.
Caso clínico
Presentamos el caso de una paciente de 67 años que acude a la consulta demandando tratamiento implantológico para el maxilar superior. Lleva varios años con prótesis removibles parciales, y ha ido perdiendo piezas de manera progresiva. Actualmente, tiene pocas piezas dentales remanentes y las que conserva tiene problemas de movilidad y dolor, por lo que consulta para poder rehabilitar con implantes la zona. En las imágenes iniciales podemos observar el estado de las prótesis removibles y los dientes naturales presentes (figs. 1-4).
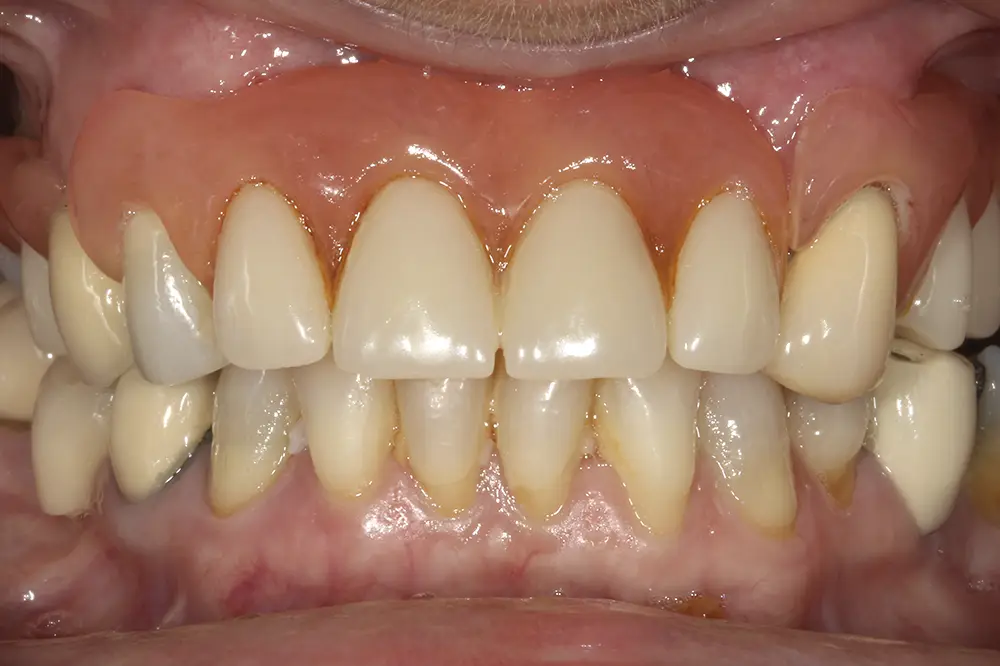
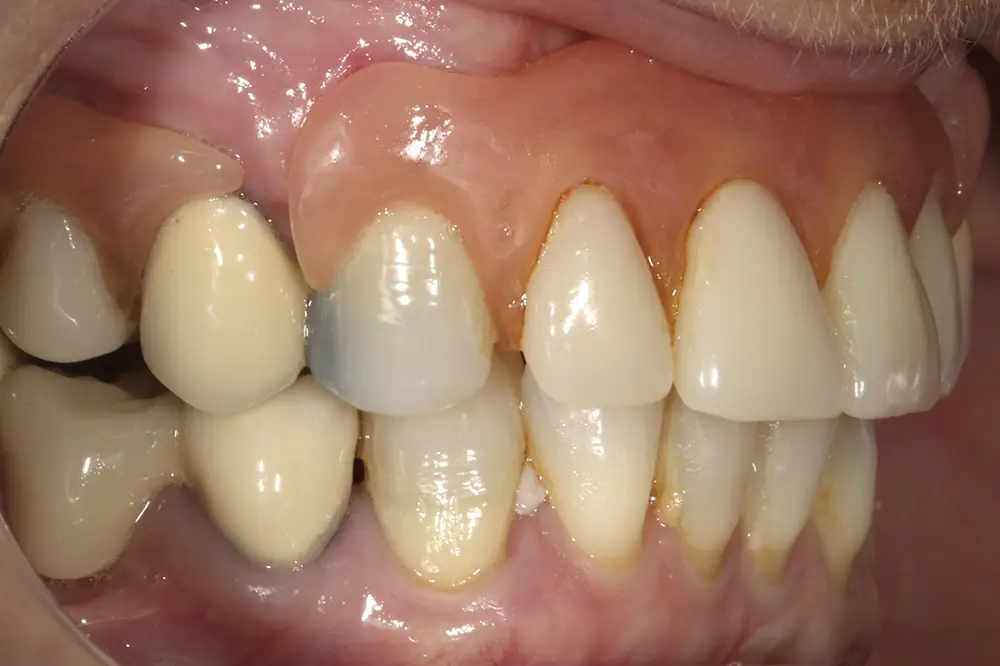
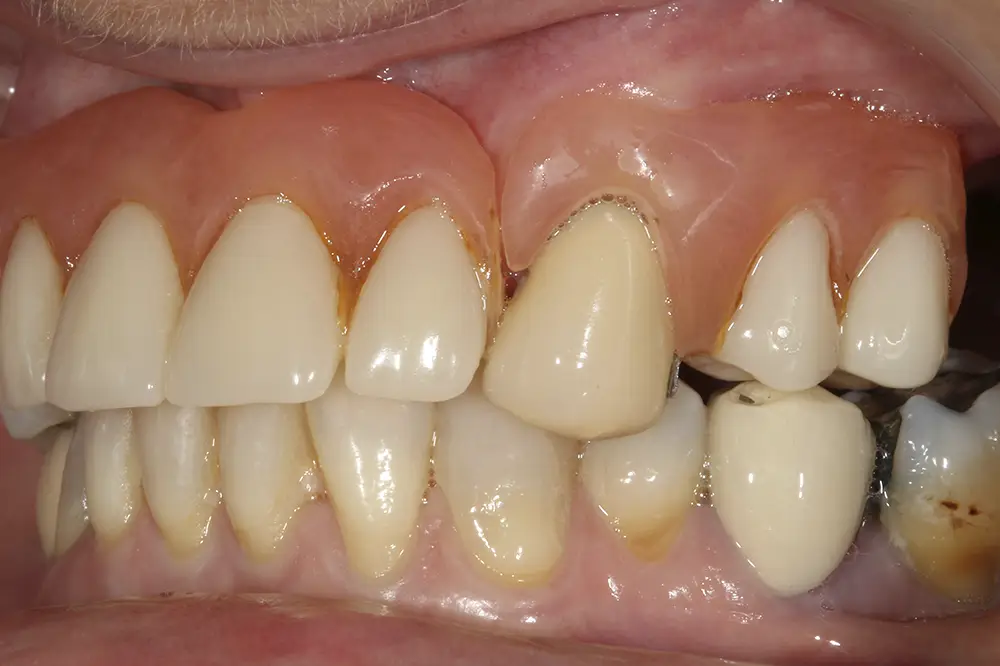
Figs. 1-4. Imágenes iniciales de la paciente, donde observamos el estado de la prótesis removible que porta la paciente frontal y lateralmente, así como los dientes remanentes.
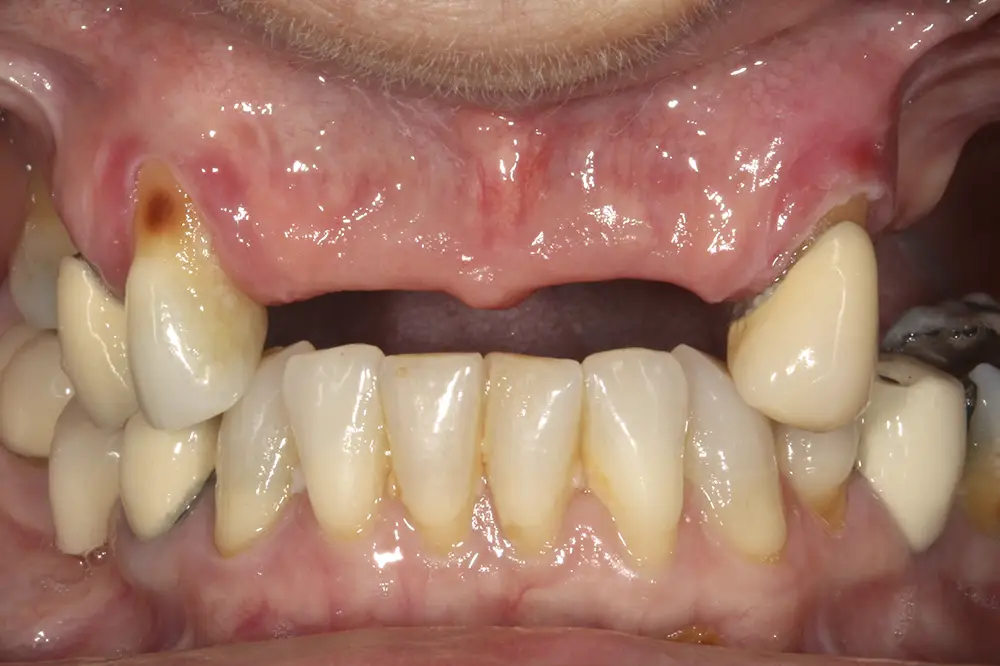
Al retirar las prótesis en las imágenes laterales, observamos además un colapso de la zona anterior y recesiones en todas las piezas que aún conserva la paciente (figs. 5 y 6). En la radiografía inicial observamos pérdidas óseas elevadas en el molar del primer cuadrante y el premolar de este mismo sector, por lo que se decide su exodoncia y regeneración con PRGF, que se realizará el mismo día de la primera fase de inserción de los implantes. En el arco inferior hay también problemas con los sectores posteriores, con pérdidas óseas en el cuarto cuadrante y signos de fractura vertical en el puente 44-46 y caries radicular en las piezas 35 y 36 (fig. 7). Por ello, estas piezas inferiores son también candidatas a la exodoncia, regeneración y reposición con implantes dentales, para lograr una posterior rehabilitación funcional.
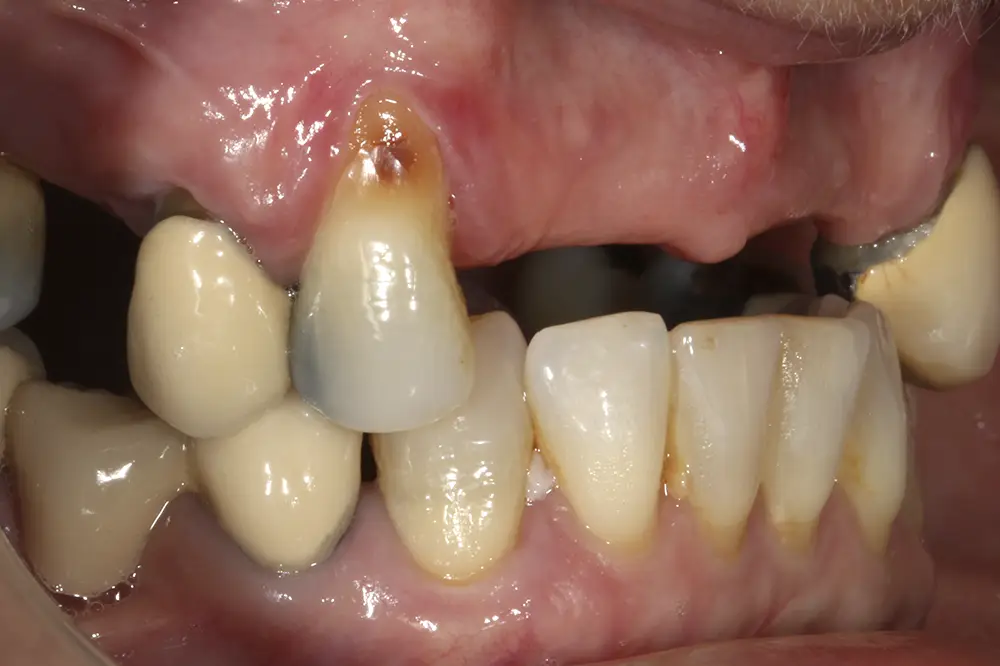
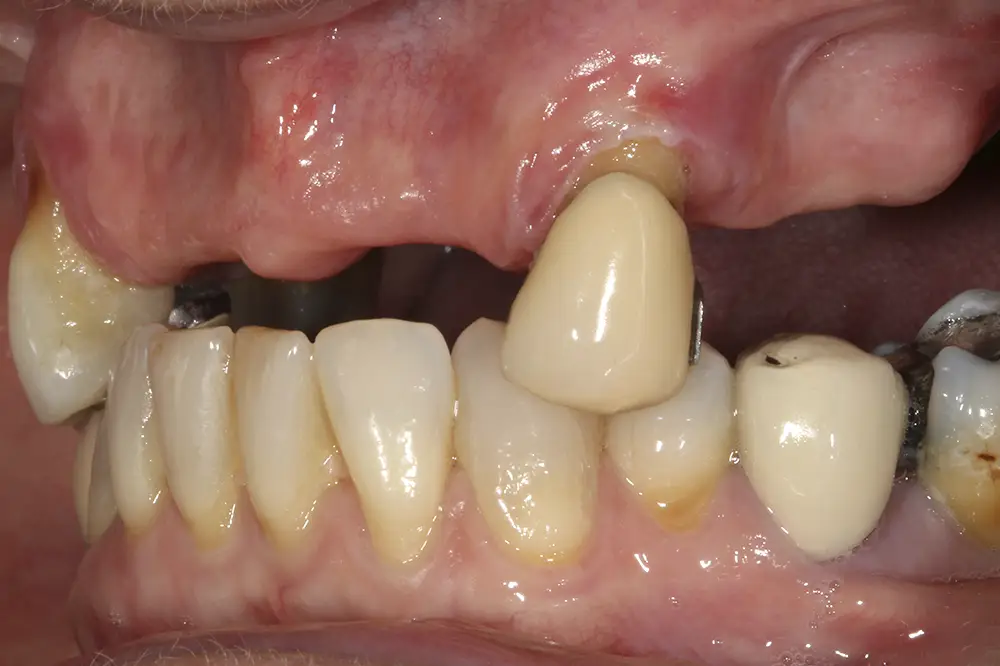
Figs. 5 y 6. Imágenes laterales de la paciente sin su prótesis. Al retirarla, se hace evidente el colapso de la dimensión vertical y la pérdida ósea y recesión de los dientes pilares que sostienen la prótesis removible.
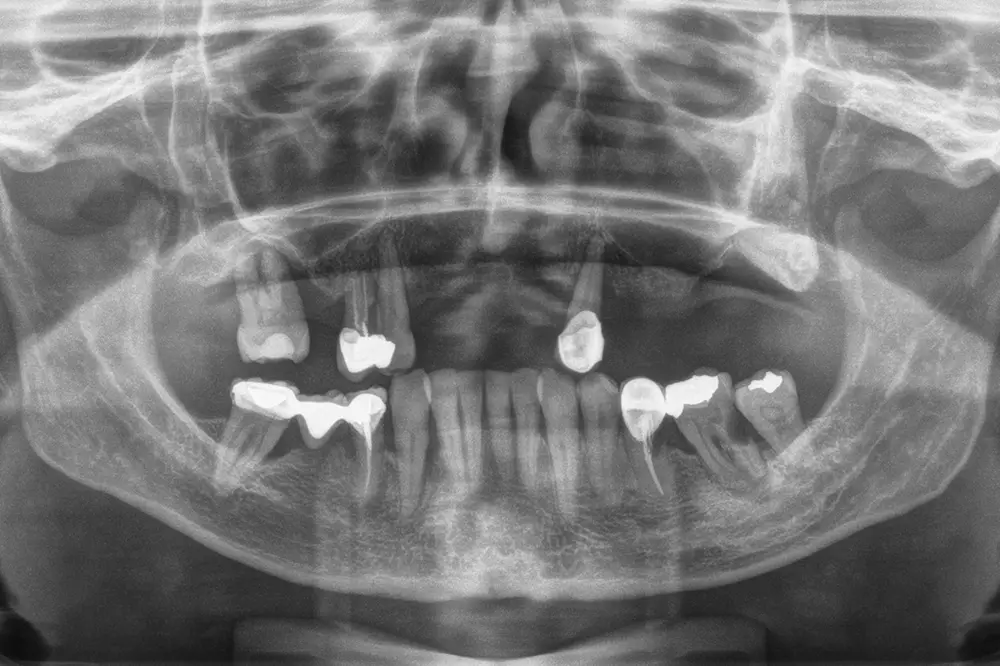
Fig. 7. Radiografía panorámica inicial del caso, donde observamos la pérdida ósea del molar remanente del primer cuadrante y el primer premolar, que deciden extraerse y regenerarse la zona con PRGF-Endoret en el momento de la cirugía de implantes. Así mismo, las piezas 35 y 36 son también candidatas a la exodoncia por fracaso del tratamiento restaurador previo.
Para realizar una planificación precisa del caso y determinar el volumen óseo residual antes de la cirugía implantológica, se realiza un estudio mediante tomografía de haz cónico (cone-beam) y se visualiza mediante un software específico (BTI-Scan IV). Esta exploración permite medir con exactitud la altura y anchura de la cresta ósea, así como evaluar la densidad de las zonas en las que se prevé colocar los implantes, facilitando así una planificación quirúrgica fiable y ajustada a las necesidades anatómicas del paciente44–47. En las imágenes del cone-beam de control, observamos en el segundo cuadrante una atrofia vertical extrema, con zonas de menos de 4 mm de altura, donde se planifican implantes de 4,5 mm de longitud que serán colocados mediante el procedimiento de elevación transcrestal con fresa de corte frontal y con hueso autólogo obtenido del fresado embebido en PRGF-Endoret como material de injerto. Esta técnica, descrita por nuestro grupo de estudio, nos permite realizar un abordaje seguro del seno maxilar con una escasa invasividad (figs. 8-10)9,25,29,36.
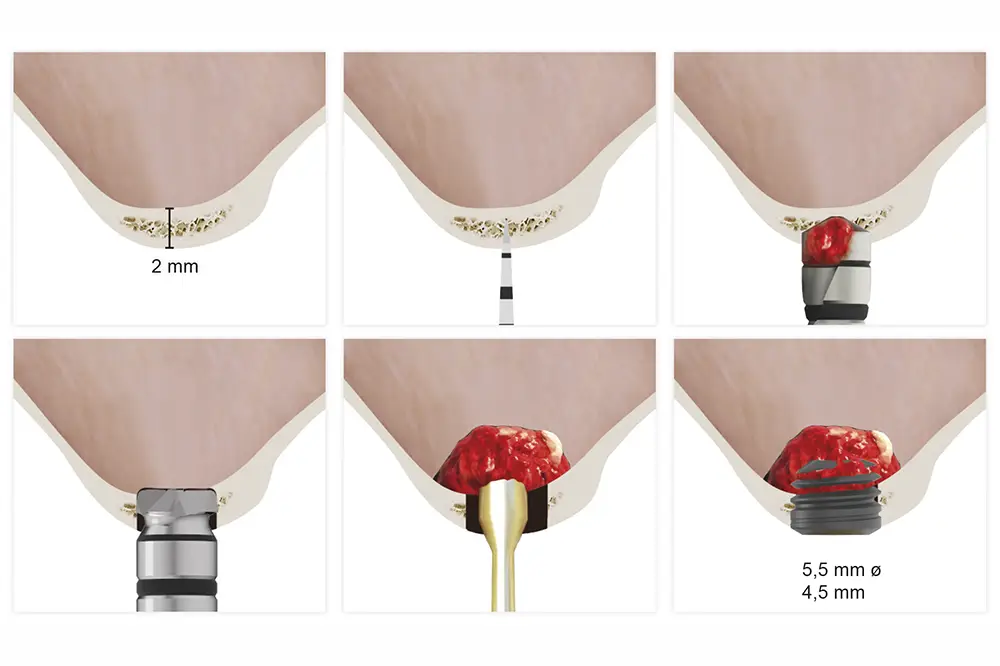
Fig. 8. Esquema de colocación de un implante de 4,5 mm de longitud en un seno con atrofia ósea extrema en altura. Se comienza con la fresa de inicio y de diámetro creciente (en función del diámetro del implante a colocar) manteniendo al menos 1 mm hasta la cortical sinusal. Finalmente se realiza el fresado de la cortical con la fresa de ataque frontal para evitar lesionar la membrana de Schneider y se despega esta desde el neoalveolo introduciendo el hueso autólogo embebido en PRGF-Endoret para finalizar con la colocación del implante.
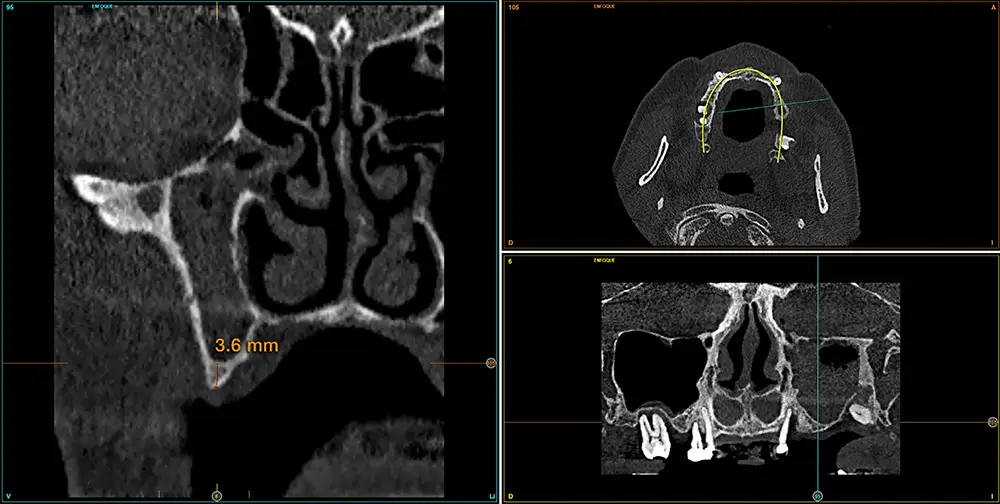
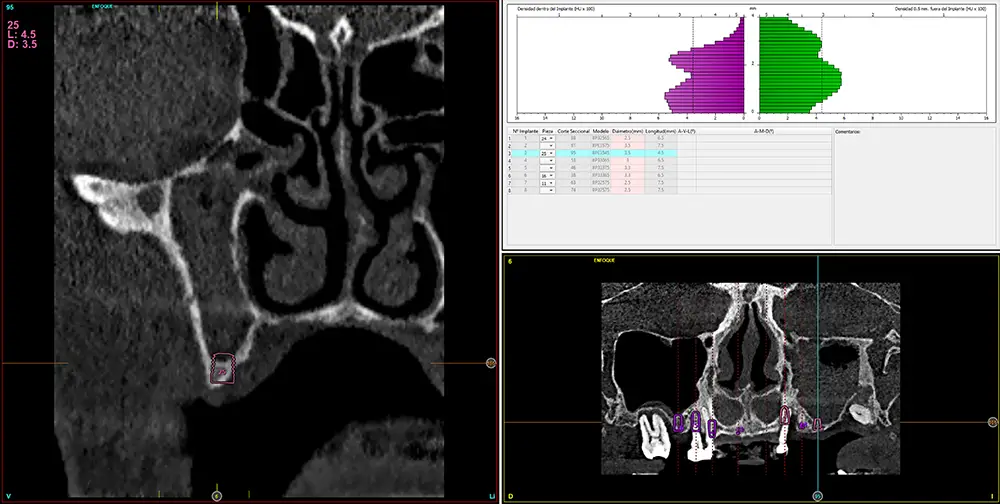
Figs. 9-10. Medida de la zona con mayor atrofia del segundo cuadrante menor a 4 mm de altura y planificación del implante de 4,5 mm de longitud que será colocado mediante el procedimiento de elevación transcrestal anteriormente descrito.
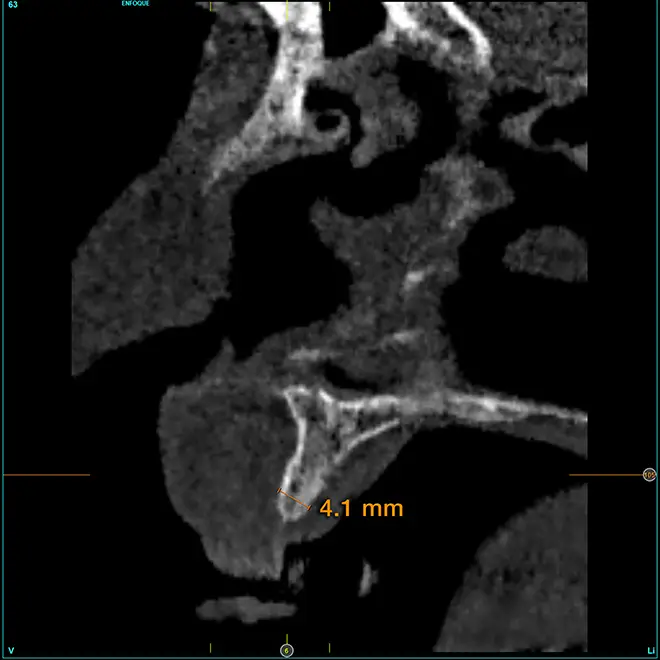
En la zona correspondiente a la pieza 24, tenemos una atrofia extrema también pero en este caso en sentido vertical, con una cresta residual de 3,1 mm de grosor, como podemos ver en el corte seccional del cone-beam (fig. 11). En este caso se planifica la colocación de un implante de 2,5 mm de diámetro y 6,5 mm de longitud (con plataforma reducida de 3 mm -plataforma 3.0, biotechnology institute-) (fig. 12). Igualmente, en la zona anterior de la premaxila, tenemos una situación muy similar donde el volumen óseo es reducido, incluso más que en la zona del segundo cuadrante y, por ello, optamos también por implantes de 2,5 mm de anchura y plataforma de 3 mm (figs. 13-16).
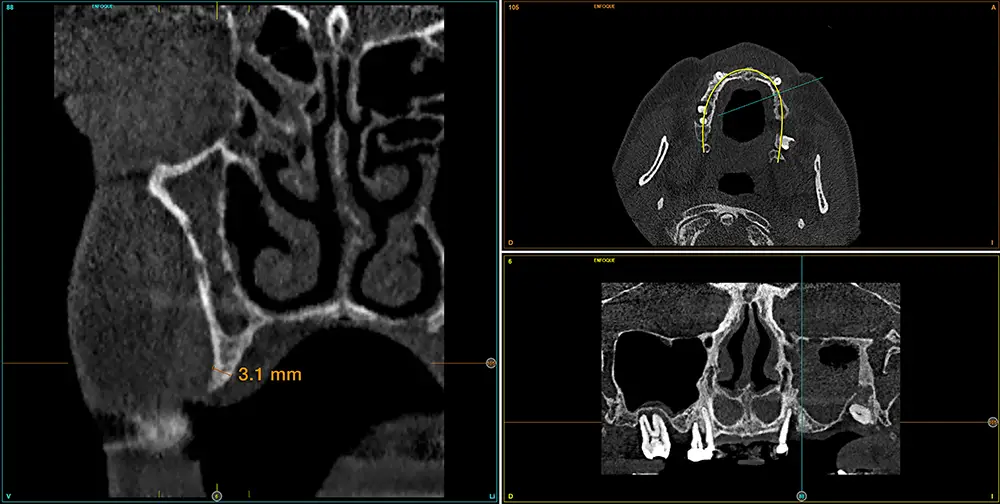
Fig. 11. Corte de planificación de la zona correspondiente a la pieza 24, que presenta una atrofia ósea en anchura extrema con 3,1 mm de anchura residual.
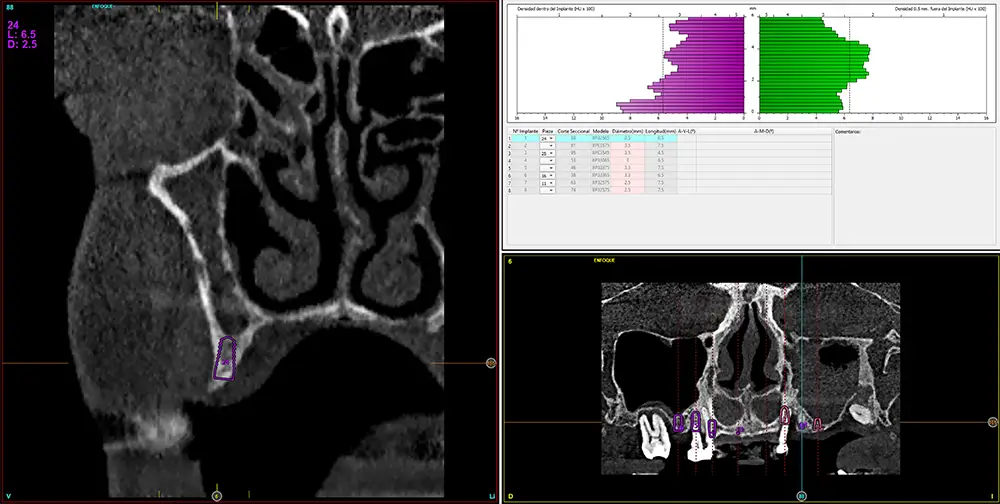
Fig. 12. Planificación del implante de 2,5 mm de diámetro y 6,5 mm de longitud que será colocado en la zona.
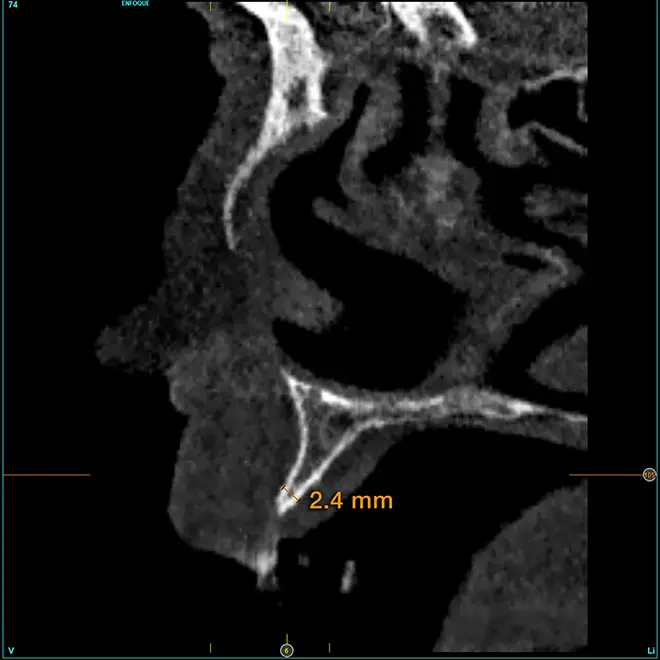
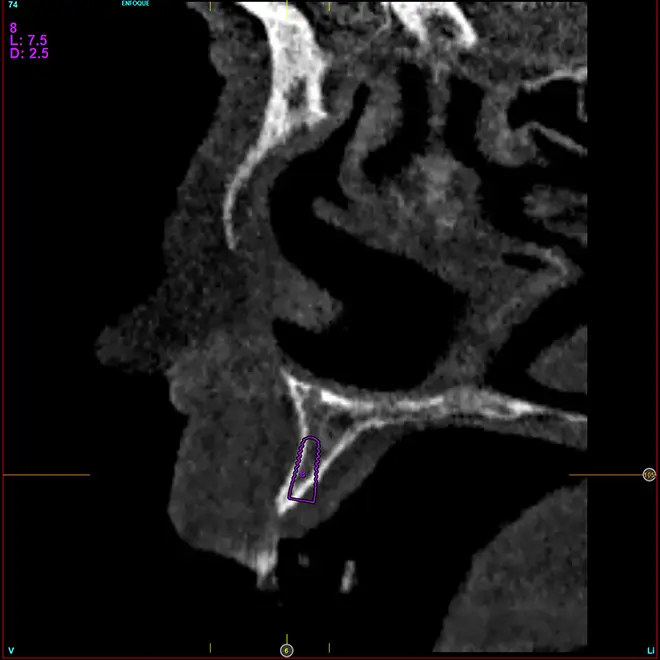
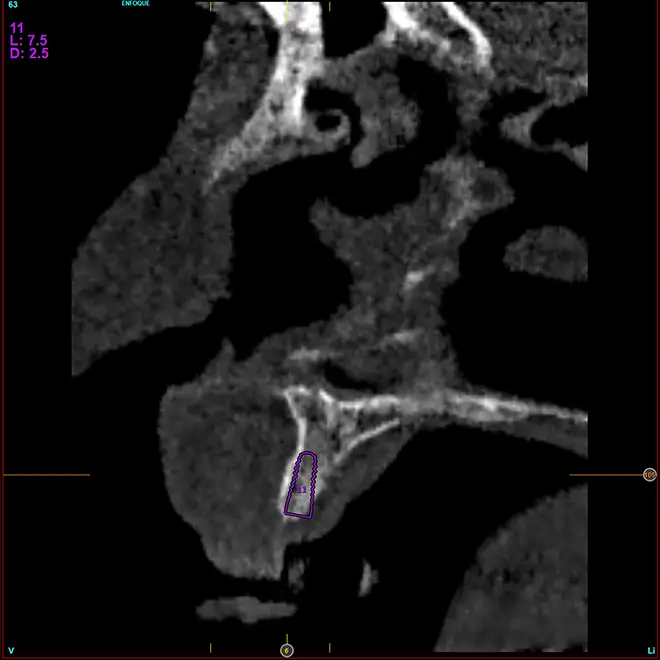
Figs. 13-16. Imágenes del cone-beam del área de la premaxila con una anchura ósea muy disminuida y la planificación de implantes de 2,5 mm de diámetro y 3 mm de plataforma.
En estas zonas de atrofia horizontal extrema, utilizamos, además de los implantes anteriormente descritos, una técnica para su colocación que consiste en la compactación y expansión del volumen óseo residual, lográndose una correcta estabilidad primaria y preservándose al máximo el volumen óseo residual en las paredes del neoalveolo. Este procedimiento se lleva a cabo con los expansores motorizados y la colocación final del implante como último expansor. Además, podemos realizar sobre la tabla vestibular una sobrecorrección final con hueso autólogo obtenido del fresado o con un rascador óseo de zonas adyacentes y finalizar con una capa de biomaterial sobre el hueso autólogo25,29,36,37,48,49. De este modo se logra una cresta de mayor anchura con un procedimiento mínimamente invasivo (fig. 17). Finalmente, en la zona distal del primer cuadrante, adyacente al molar que será extraído y regenerado su alveolo con PRGF-Endoret, se planifica un implante corto de 6,5 mm de longitud y 3,3 mm de diámetro de forma directa para evitar realizar una elevación de seno a este nivel (fig. 18).
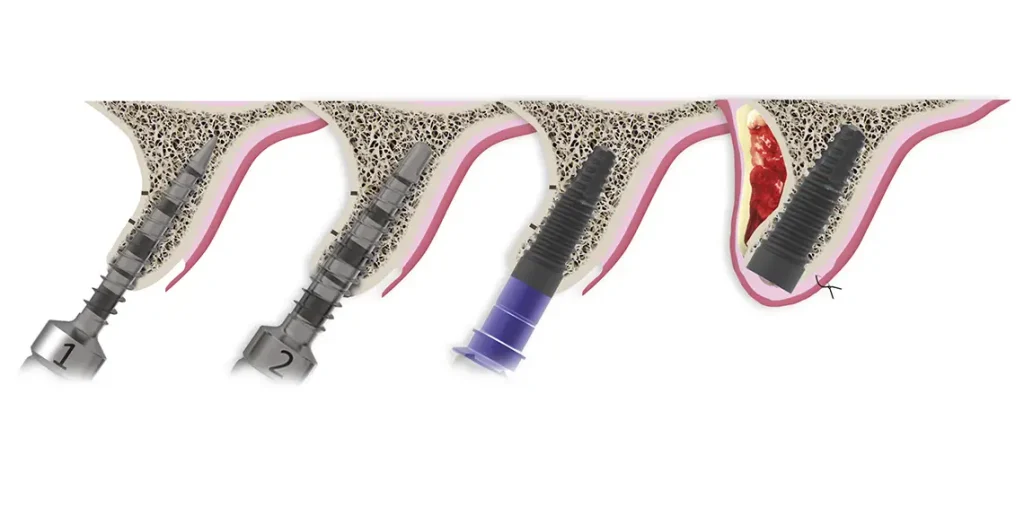
Fig. 17. Expansión del reborde alveolar residual con extrema atrofia en anchura con los expansores motorizados y la colocación del implante como expansor final, añadiéndose una sobrecorrección vestibular posterior para corregir la atrofia ósea transversal.
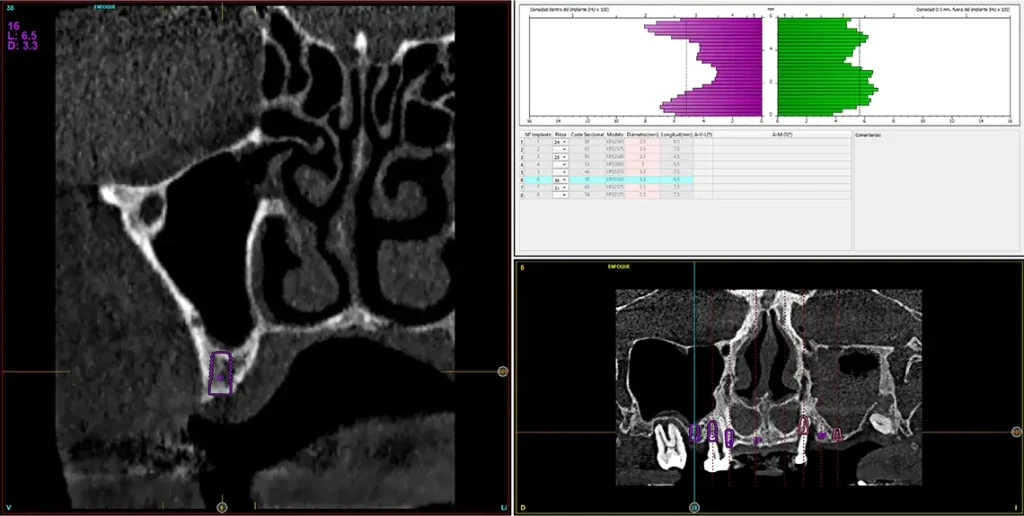
Fig. 18. Planificación del implante del primer cuadrante en la zona adyacente al molar que será extraído, que se colocará para evitar la elevación de seno en este nivel.
Una vez realizada la planificación de forma exhaustiva, y analizadas las técnicas quirúrgicas e implantes que se van a emplear en cada zona del maxilar superior, se procede a la cirugía de implantes. Para realizar una inserción de los mismos guiada a través de la prótesis, se confecciona una guía quirúrgica que nos sirve de referencia durante la cirugía, que se posicionará en los caninos superiores que se deciden mantener para la fase de provisionalización del paciente (figs. 19-22). Tal como se ha explicado, podemos observar en las imágenes de la cirugía la sobrecorrección que se lleva a cabo de las zonas con mayor atrofia a nivel horizontal (figs. 23-24). Tras la cirugía, los implantes se dejan en dos fases quirúrgicas, debido al empleo de técnicas accesorias y se coloca un provisional sobre los dos caninos que se conservan temporalmente (figs. 25-26). Estos caninos que se conservan se tratan mediante tratamiento periodontal quirúrgico para una mejor cicatrización postoperatoria y alargar la vida de los mismos el tiempo que se necesita para los provisionales.
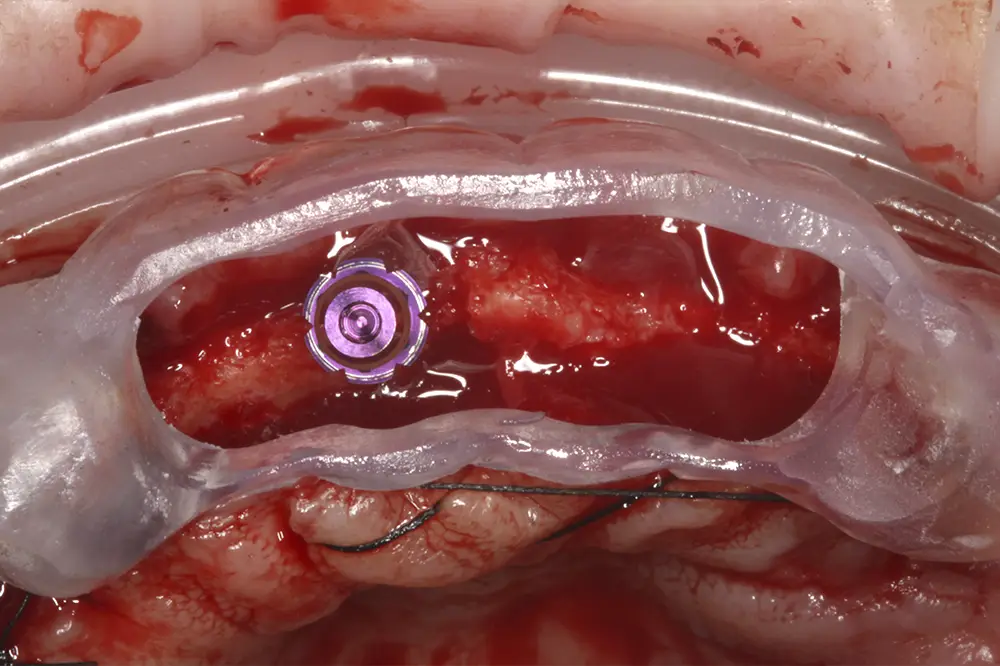
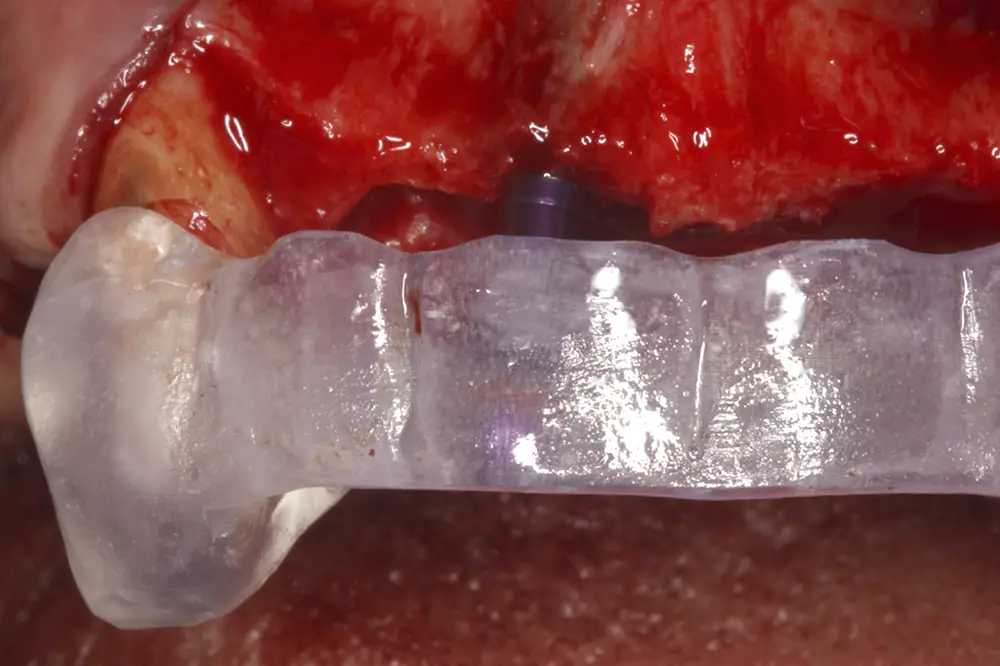
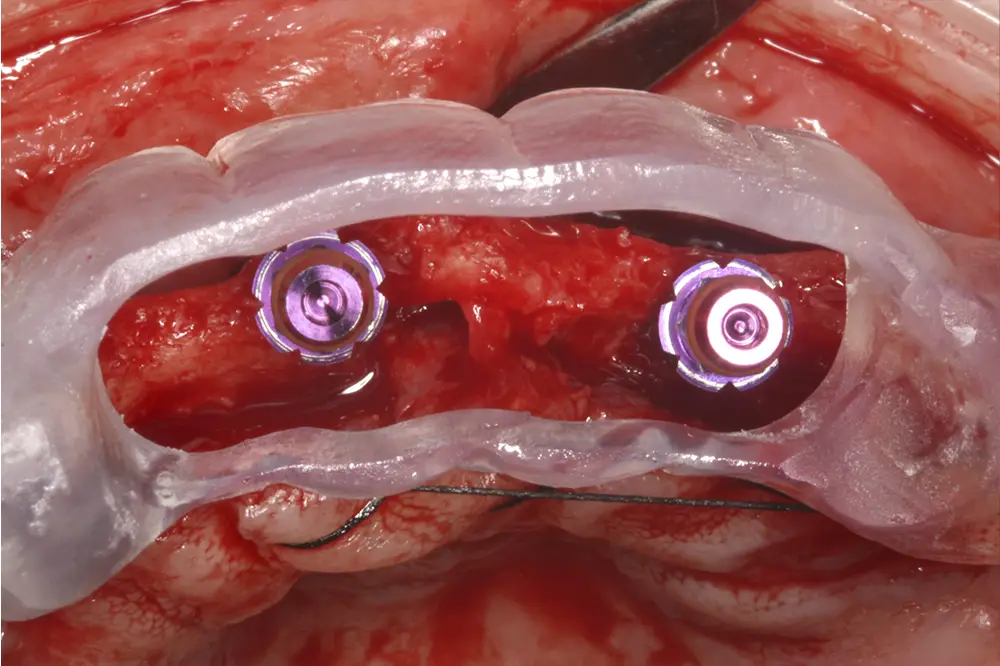
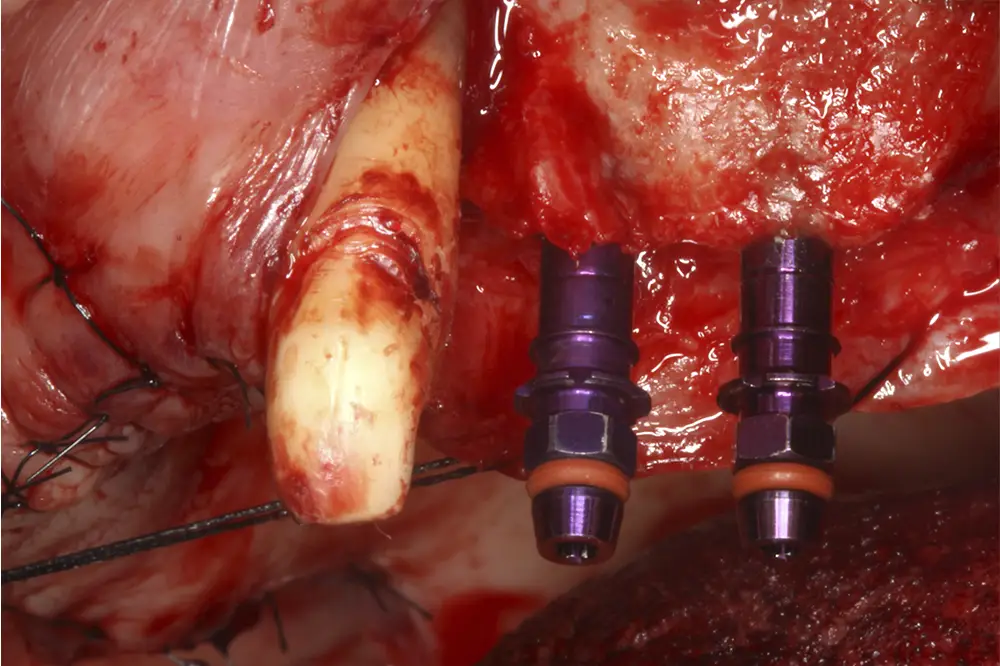
Figs. 19-22. Colocación de los implantes posicionándose tridimensionalmente a través de la guía quirúrgica.
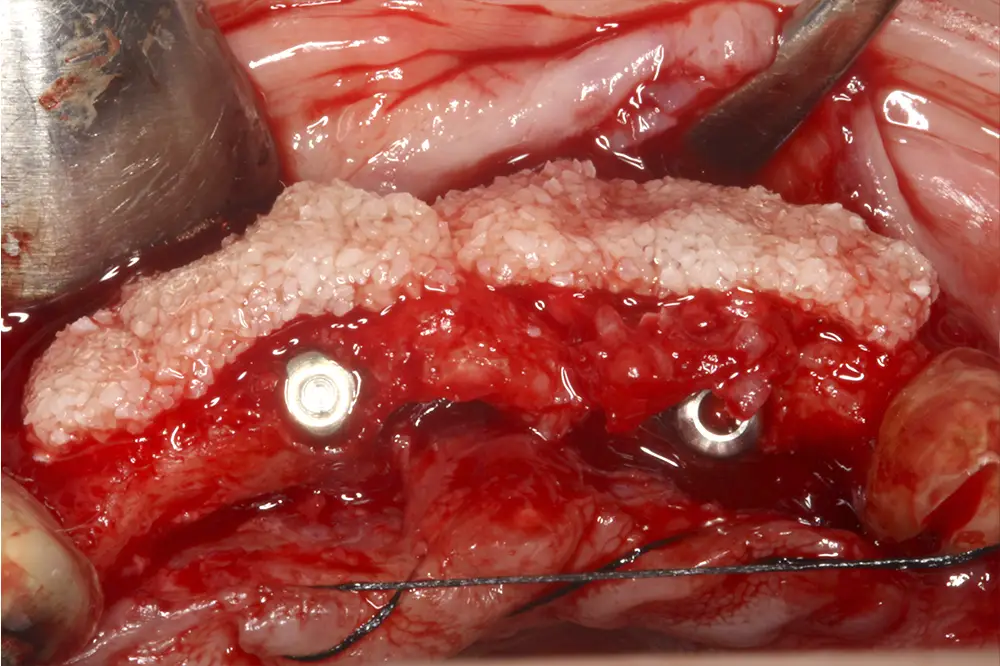
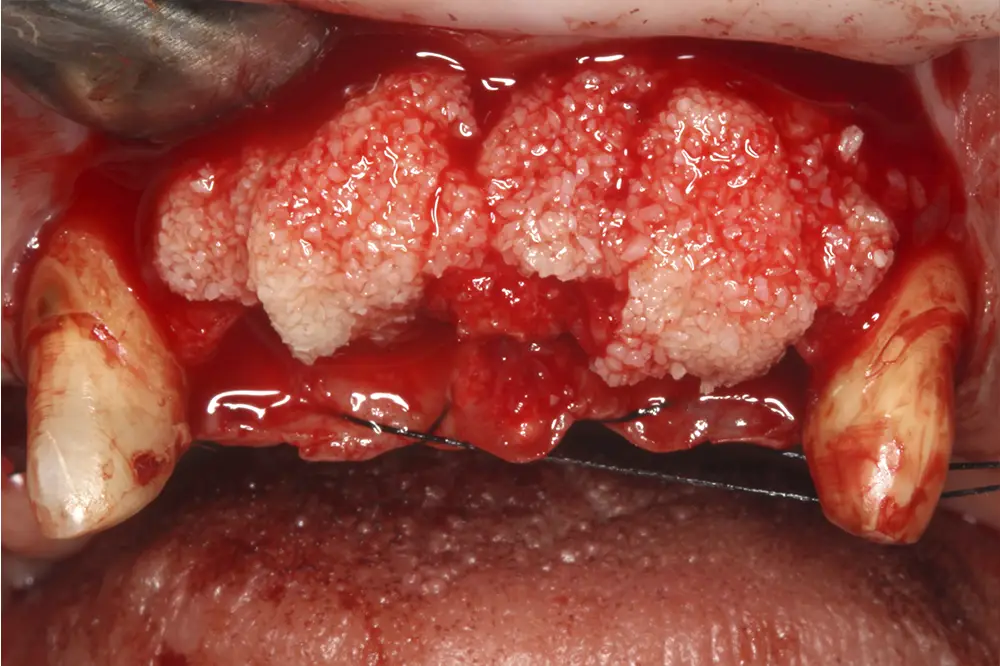
Figs. 23 y 24. Sobrecorrección posterior según el protocolo anteriormente descrito, donde se coloca el hueso autólogo con PRGF-Endoret en la capa basal y el biomaterial en la superior. Posteriormente, se cubre todo con membranas de fibrina autóloga retraídas y se sutura sin tensión con un monofilamento 5/0.
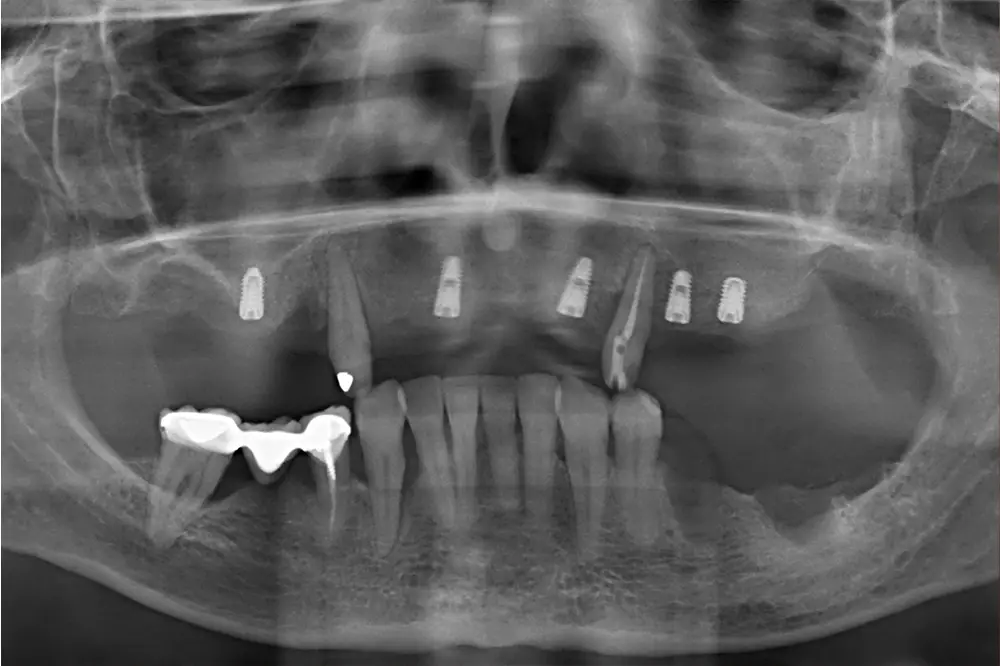
Fig. 25. Radiografía postquirúrgica tras las exodoncias y la colocación de los implantes con las diferentes técnicas comentadas anteriormente.
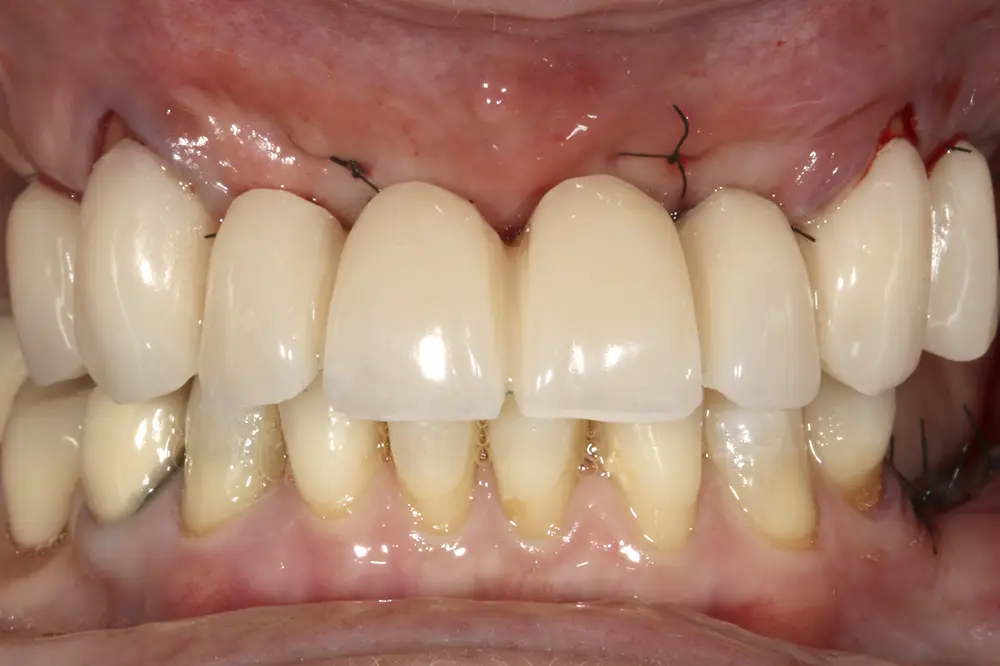
Fig. 26. Provisional sobre los caninos para cicatrización sin presión de los implantes recién colocados.
Transcurridos cuatro meses desde la fase inicial, ya tenemos suficiente hueso disponible en las zonas donde se realizaron las extracciones y regeneraciones con PRGF-Endoret, por lo que podemos planificar la colocación de implantes en estas áreas en un segundo tiempo quirúrgico. En el primer cuadrante, en los cortes del cone-beam realizado en este momento podemos observar una regeneración completa del alveolo tanto del molar como del premolar extraídos en la primera fase y cómo podemos colocar implantes, cortos y estrechos también en estas localizaciones (figs. 27-28). En esta fase, se aprovecha además para extraer los dos caninos que han cumplido con su función de permanecer durante la fase inicial de provisionales y cargar ya los implantes superiores de la primera fase con una prótesis atornillada mediante transepitelial múltiple y una estructura de barras articuladas, que permitirá de forma sencilla posteriormente ir añadiendo aquellos implantes que quieran cargarse seguidamente sin necesidad de repetir la estructura completa (figs. 29-31).
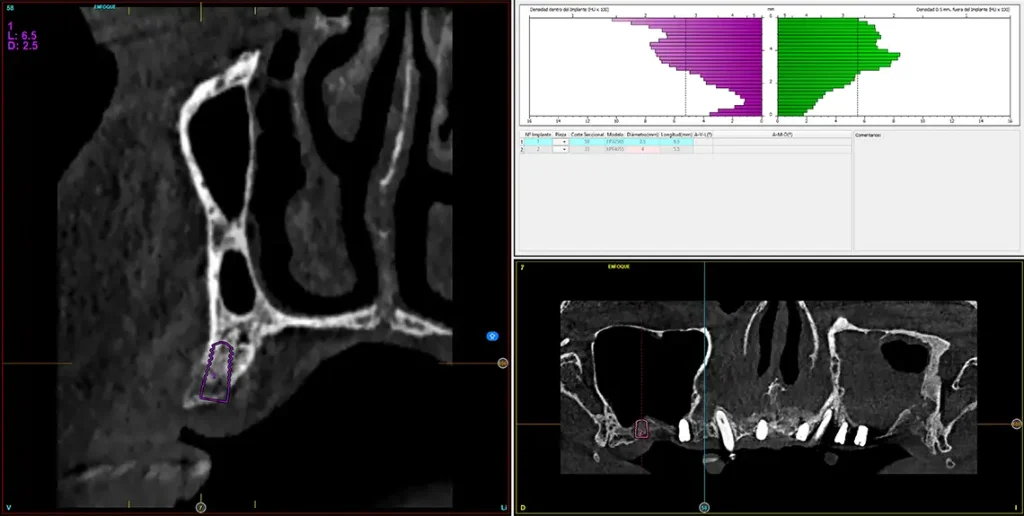
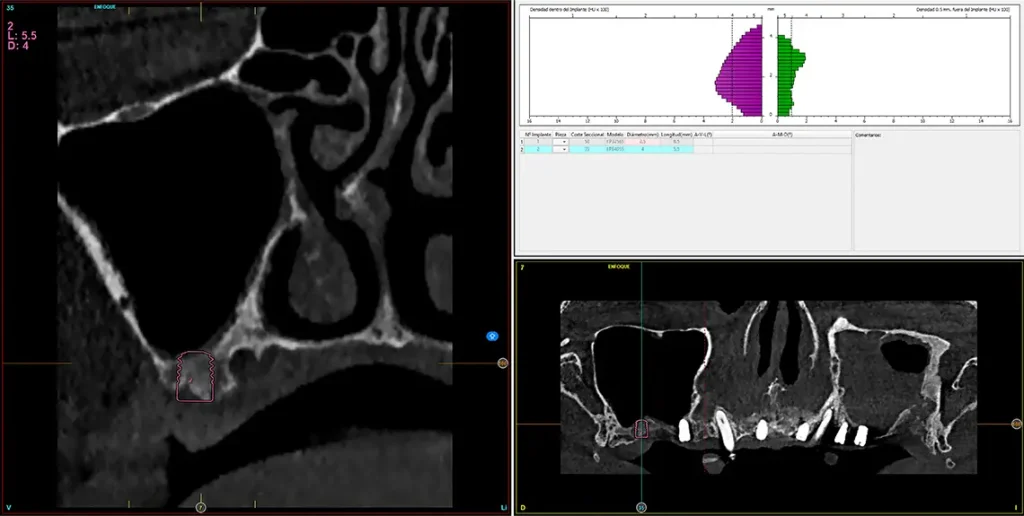
Figs. 27 y 28. Planificación de los implantes que serán colocados en el primer cuadrante tras la regeneración de los alveolos postexodoncia con PRGF-Endoret.
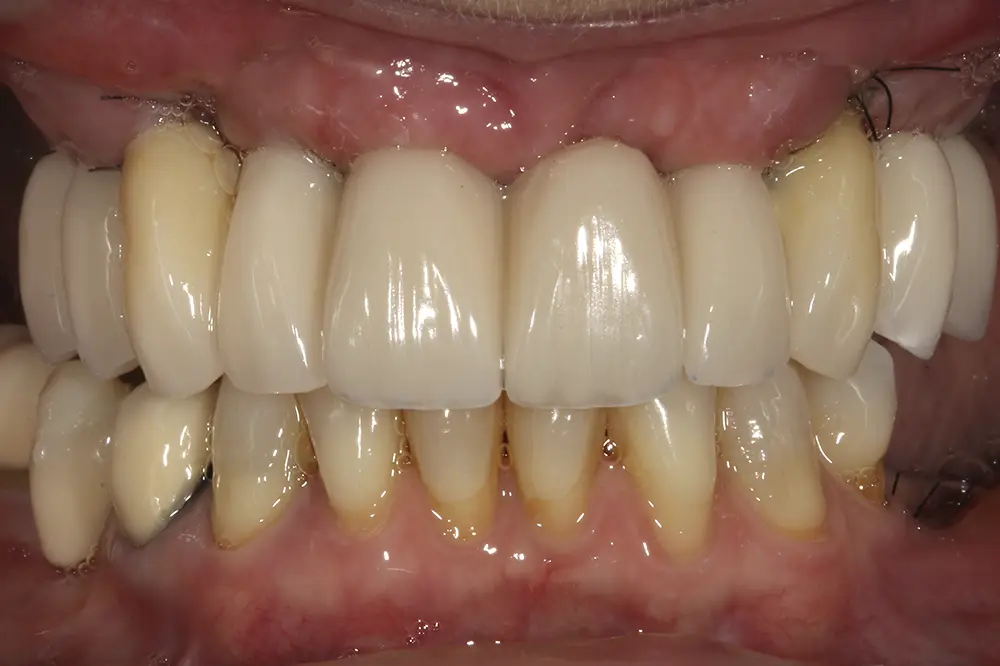
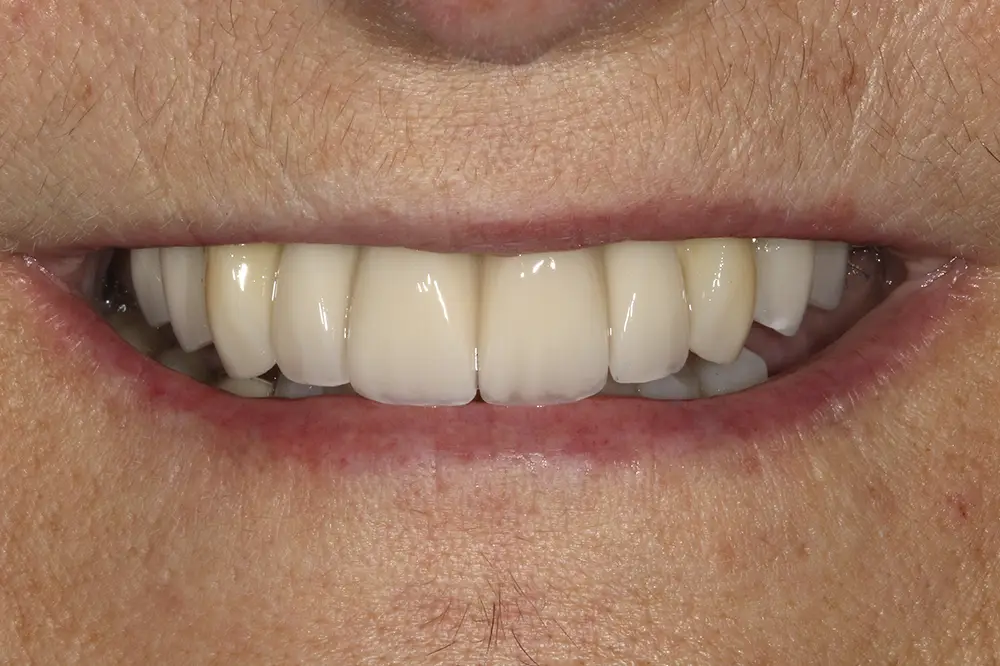
Figs. 29-30. Imágenes de la prótesis de carga progresiva, ya apoyada sobre los implantes superiores.
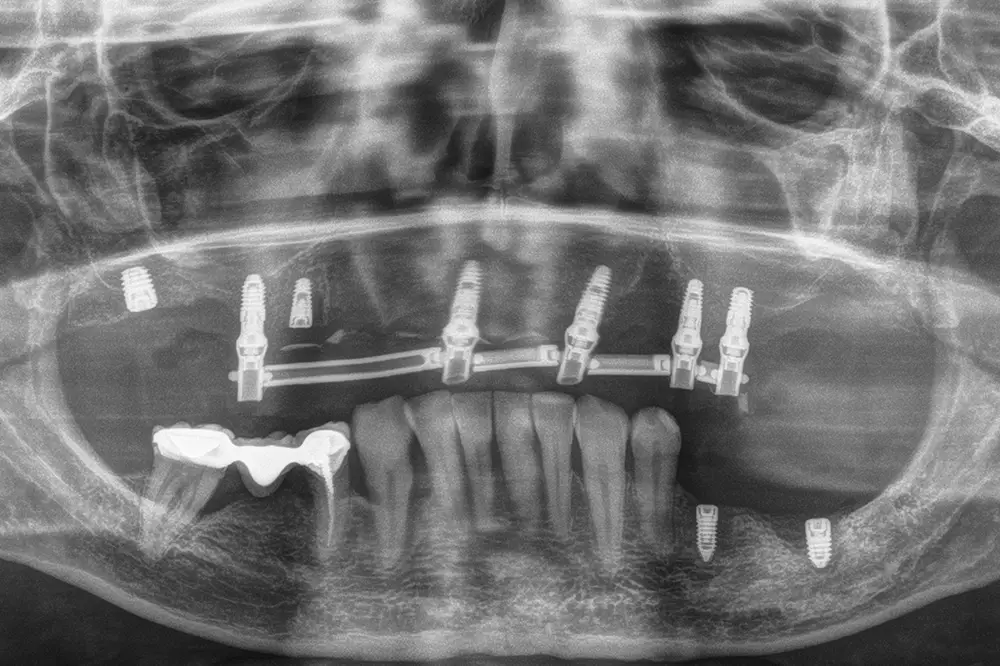
Fig. 31. Imagen de la carga de los implantes superiores de la primera fase y los dos colocados en esta segunda fase que se dejarán en dos tiempos. En este punto se lleva a cabo también la exodoncia de los caninos.
La prótesis se mantiene durante otros cuatro meses, tiempo suficiente para la regeneración de los alveolos de los caninos, donde se planifican nuevos implantes, al igual que en la zona más posterior del segundo cuadrante, donde ahora planificamos un nuevo implante extracorto con elevación de seno transcrestal (figs. 32-34). Estos implantes nos permitirán confeccionar una rehabilitación mucho más eficiente desde el punto de vista de la biomecánica y distribución de ferulizaciones. Una vez insertados, se unen a la carga implantes de la fase anterior generándose un nuevo juego de provisionales (figs. 35-37).
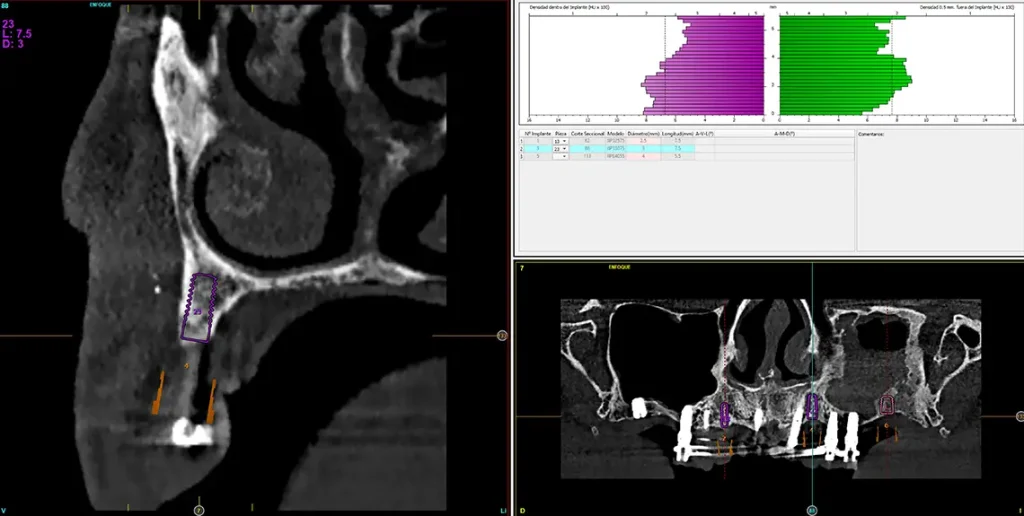
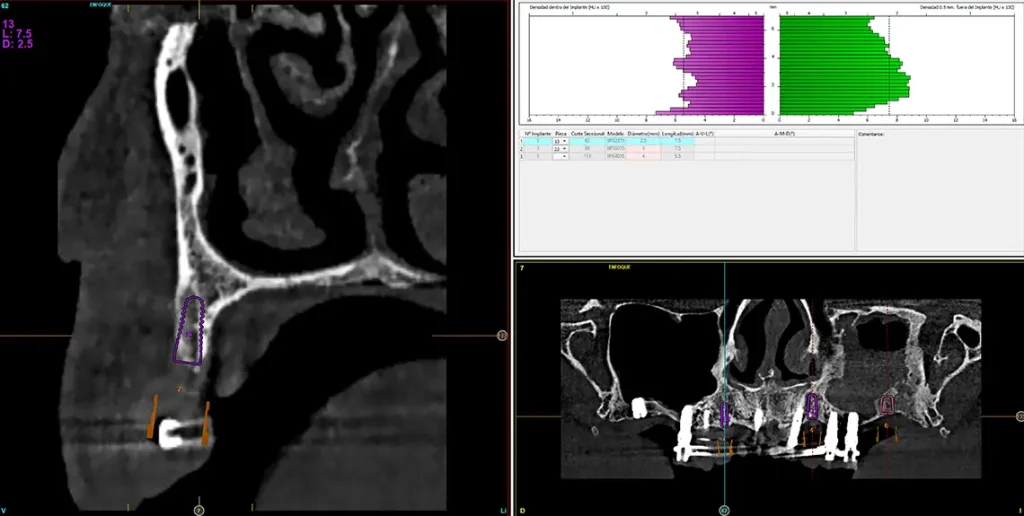
Figs. 32 y 33. Imágenes de planificación de los implantes que se colocarán en los alveolos de los caninos completamente regenerados con el uso de PRGF-endoret.
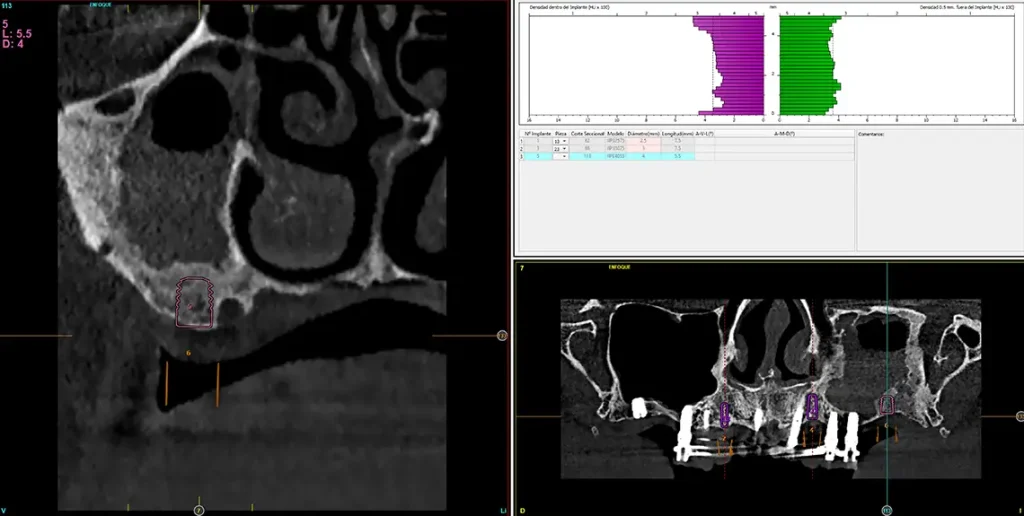
Fig. 34. Imagen de planificación del último implante del segundo cuadrante necesario para terminar la rehabilitación con un buen comportamiento biomecánico.
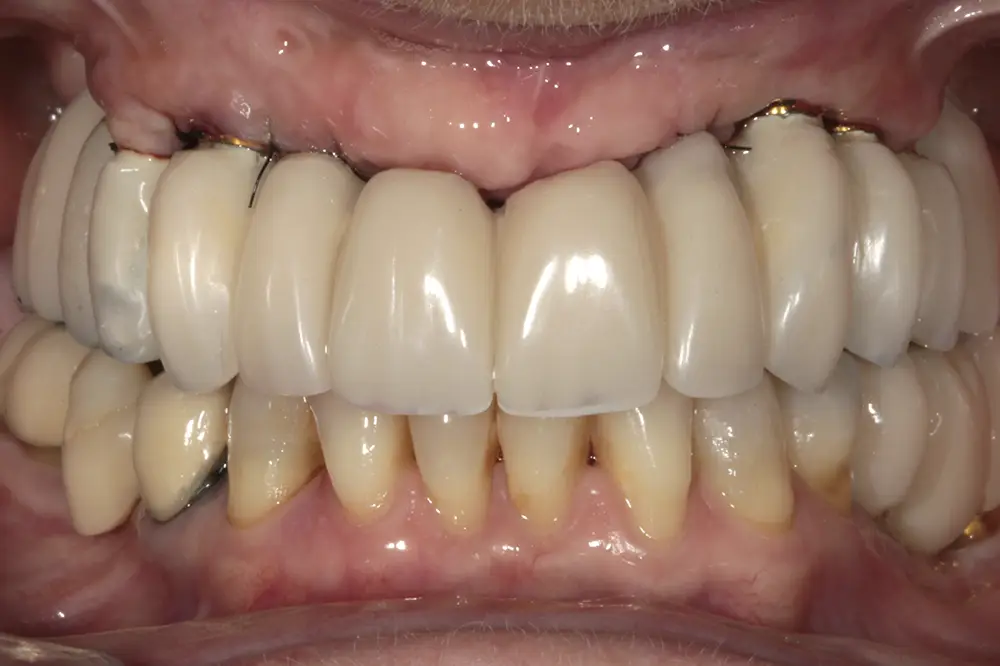
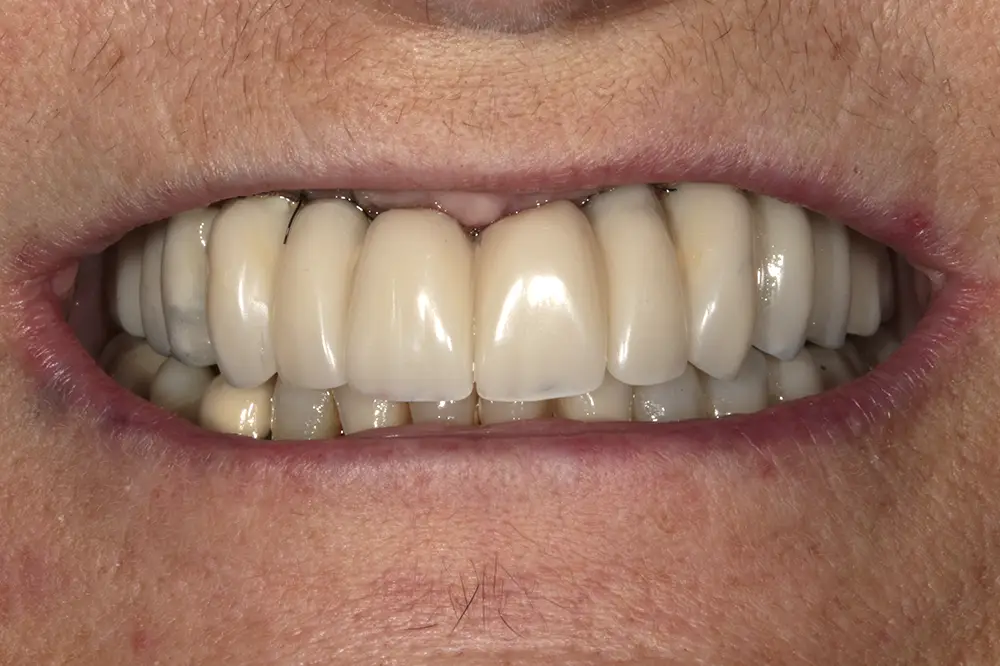
Figs. 35-36. Nuevo juego de prótesis de carga progresiva.
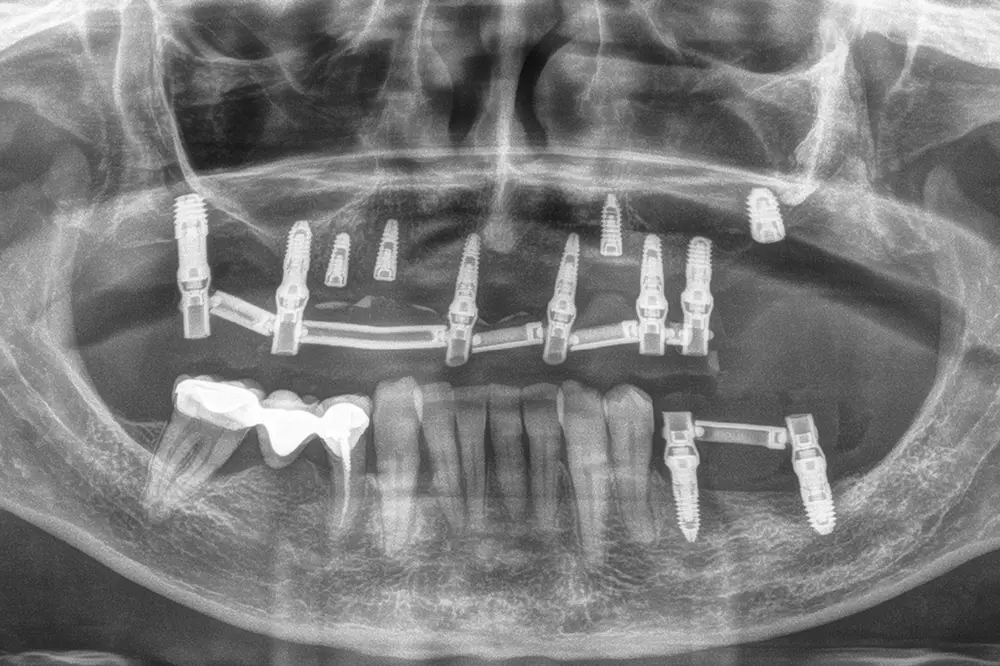
Fig. 37. Radiografía con la nueva adaptación de la prótesis de carga progresiva uniéndose los implantes de la fase quirúrgica anterior.
Transcurridos de nuevo cuatro meses más desde la última cirugía, se confecciona una prótesis de carga progresiva que engloba todos los implantes. El implante situado en la posición 22, colocado en la primera fase quirúrgica, es explantado en este momento, tratado por lo tanto como implante transicional que permitió la carga progresiva en los primeros momentos, siendo prescindible actualmente desde el punto de vista biomecánico para una mejor confección de la prótesis final (fig. 38). Esta carga se mantiene durante 2 meses más, momento en el cual se comienza la confección de la prótesis definitiva. Para ello, se realiza como primer paso el encerado diagnóstico, que se prueba en la paciente trasladando la oclusión lograda con la fase de provisionalización y mejorando aquellos parámetros que se consideran necesarios (figs. 39 y 40).
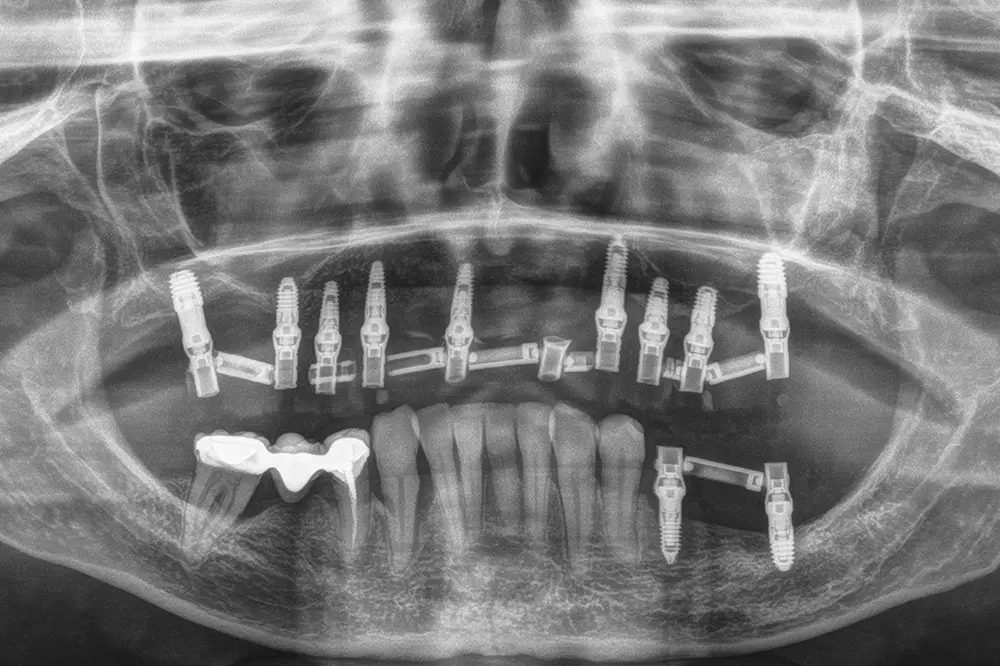
Fig. 38. Carga progresiva final de todos los implantes que englobarán la prótesis definitiva.
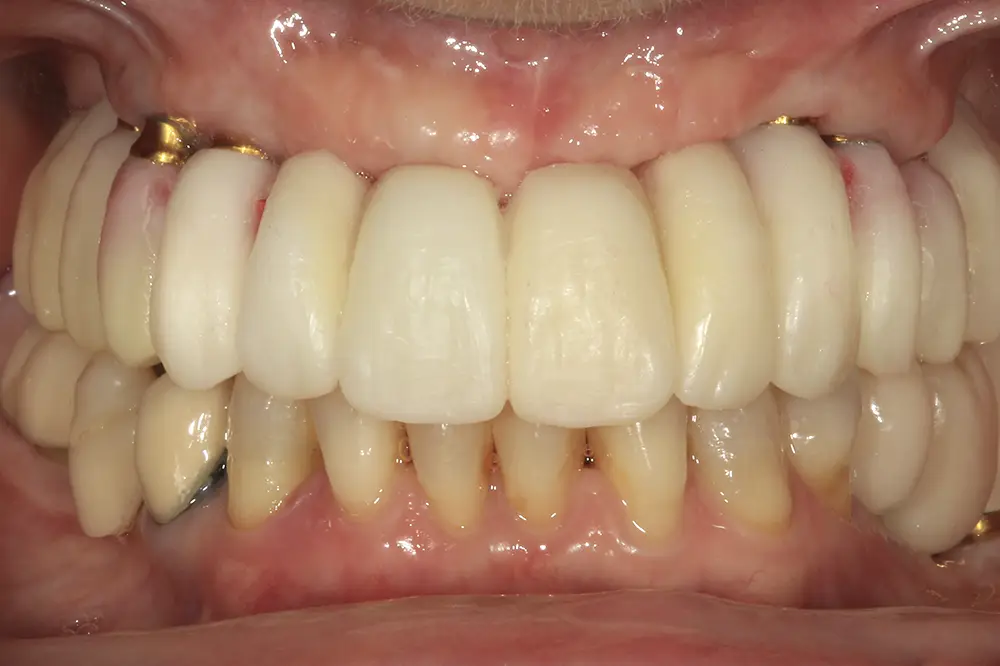
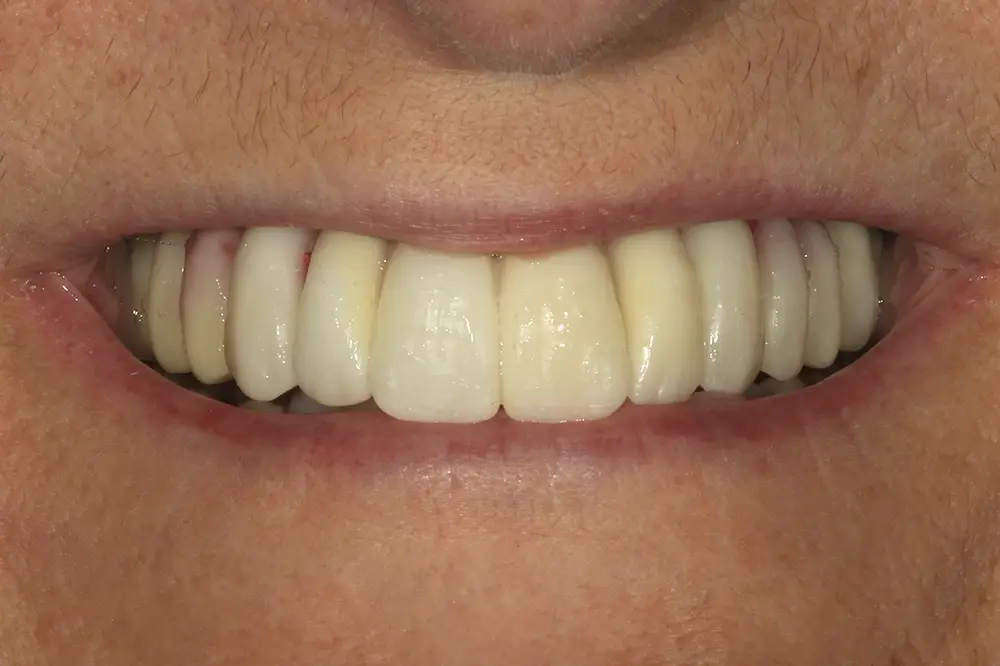
Figs. 39 y 40. Imágenes de la prueba del encerado para la confección de la prótesis definitiva.
En el diseño de la prótesis final, se optó por la realización de una prótesis en tres tramos. En la zona anterior, se diseñó una barra Blender debido a las ventajas biomecánicas y protésicas que ofrece frente a una estructura metal-cerámica convencional. Para la confección de esta prótesis del sector anterior, se digitalizaron los modelos maestros con un escáner de sobremesa 3Shape F8 (3Shape, Copenhague, Dinamarca), generando archivos STL. El diseño de la estructura metálica tipo Blender se realizó mediante software Blenderfordental® (Blenderfordental, UAE), para configurar una estructura de titanio grado V (espesor mínimo 1,5–2,0 mm) con espacio higiénico mínimo de 1 mm. Se diseñaron e incorporaron macroretenciones y, tras confirmar el ajuste pasivo entre la estructura de titanio y el recubrimiento fresado de zirconio, la estructura se sometió a un tratamiento de nitrurado para su finalización (figs. 41-44).
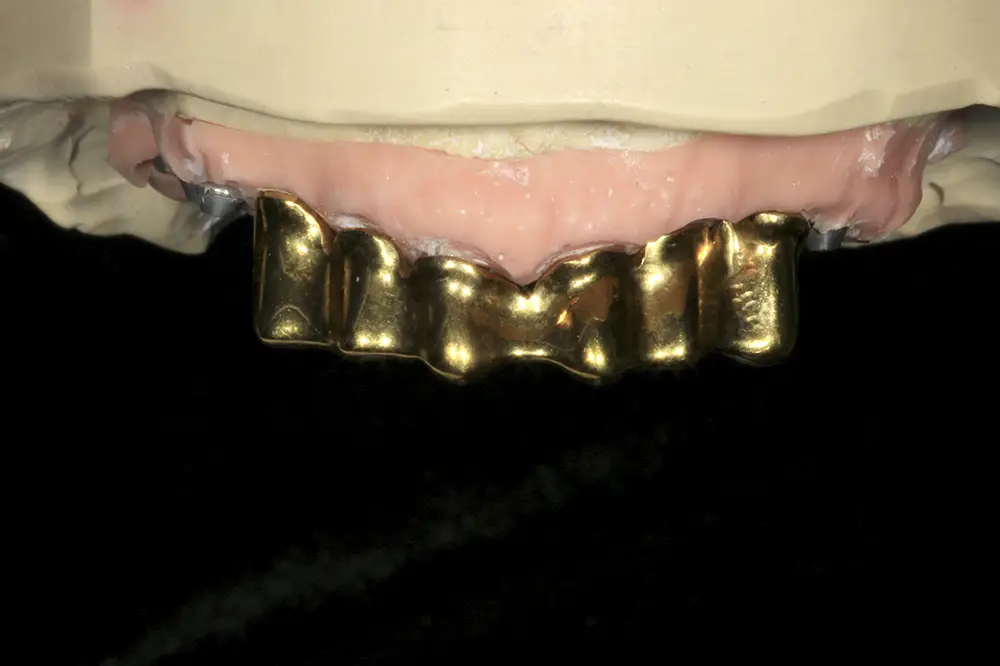
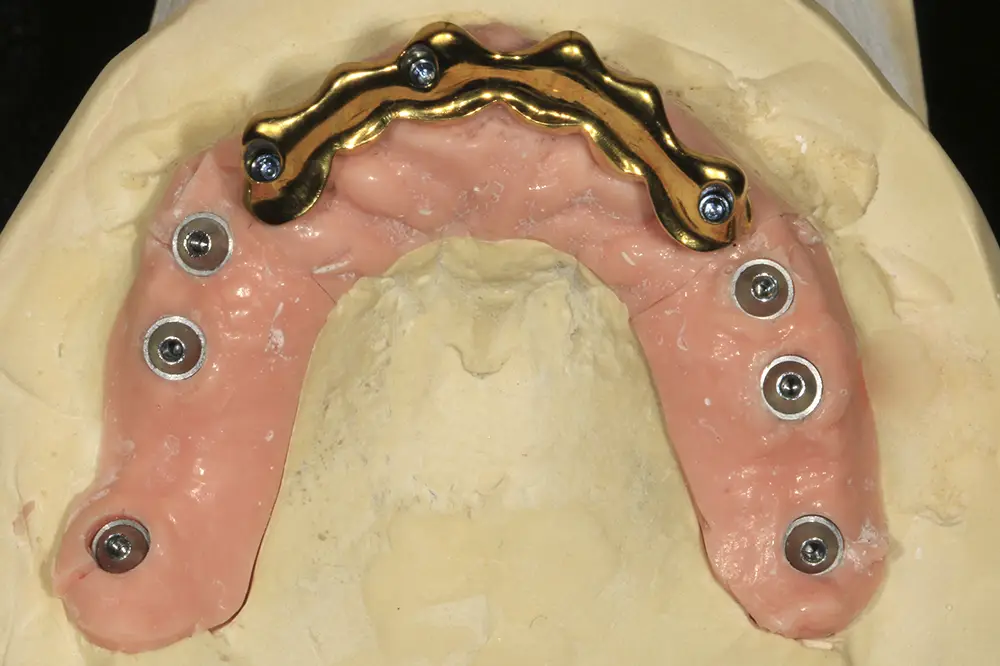
Figs. 41 y 42. Confección, nitruración y prueba en el modelo maestro de la barra tipo Blender.
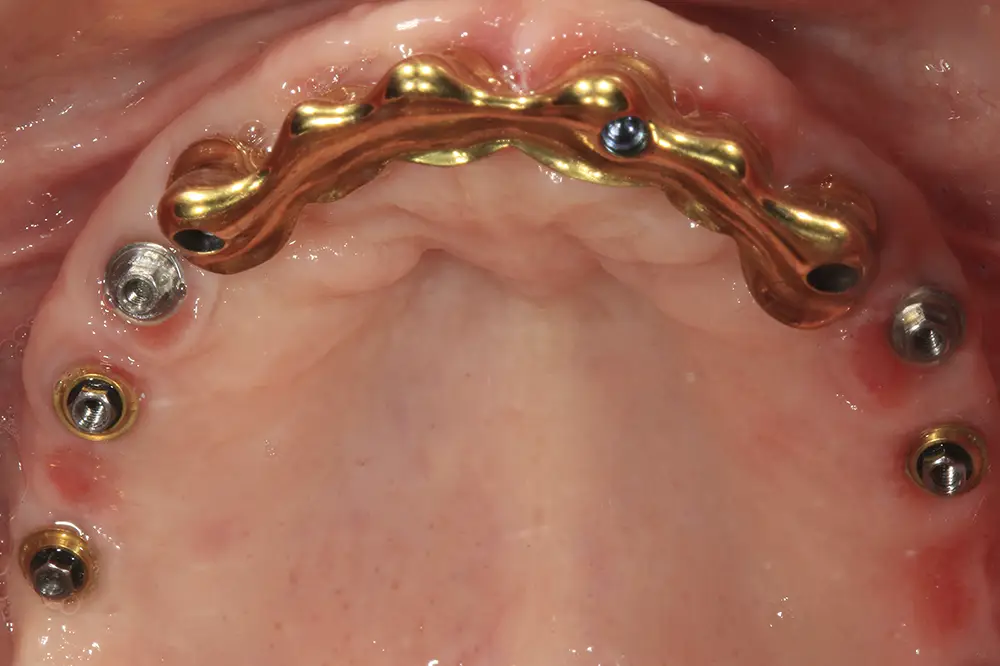
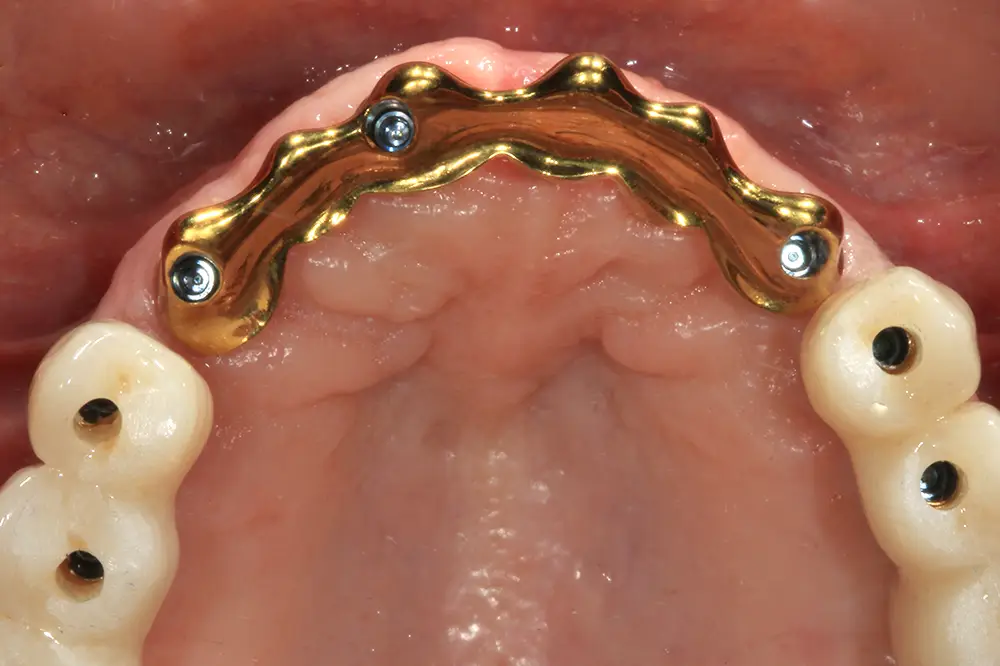
Figs. 43 y 44. Prueba de la estructura en la paciente, al igual que las prótesis del sector posterior para garantizar el correcto ajuste.
La estructura metálica de titanio y el recubrimiento fresado de zirconia se confeccionaron de forma paralela y simultánea a partir de los mismos archivos CAD. Las estructuras se fabricaron mediante fresado CAD/CAM de 5 ejes en titanio grado 5 (Ti-6Al-4V) (HTL Cad-Cam Lab, Vitoria, España). Una vez acabadas ambas piezas, se realizaron los ajustes finos necesarios hasta obtener un asentamiento pasivo y congruente entre la estructura y el recubrimiento. A continuación, la estructura metálica se envió a nitrurar y, tras el tratamiento, el recubrimiento de zirconia se cementó sobre la estructura empleando un cemento de resina autoadhesivo RelyX™ Unicem 2 Automix (3M ESPE, Seefeld, Alemania), cemento de resina autoadhesivo de curado dual siguiendo el protocolo e indicaciones del fabricante (figs. 45 y 46).
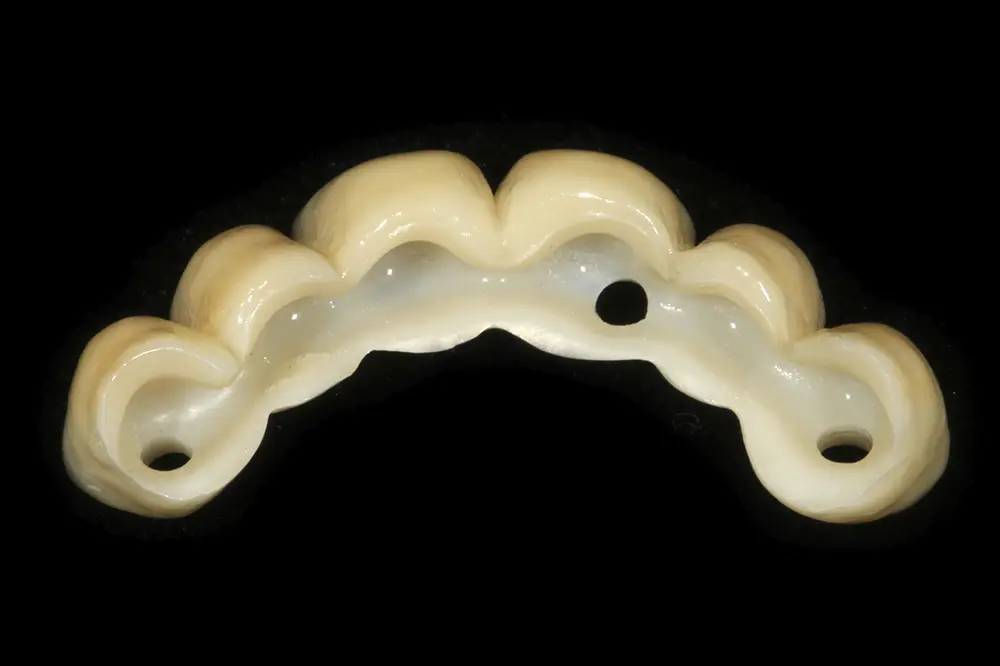
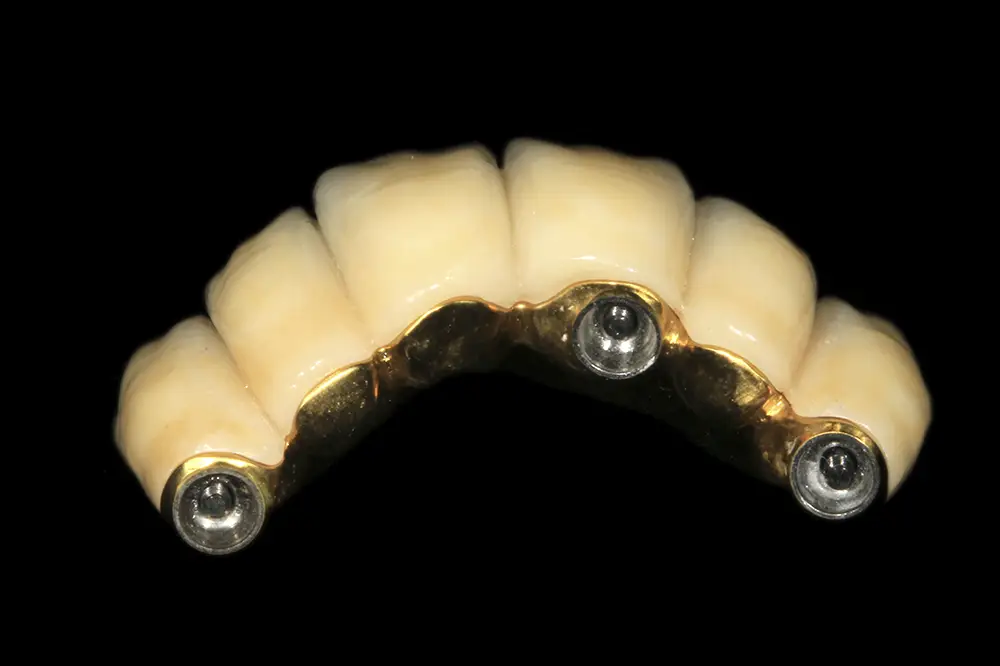
Figs. 45 y 46. Imágenes de la barra y la estructura en zirconio antes y después de unirlas mediante el cementado en frío.
Para los sectores posteriores, se fabricaron estructuras mediante fresado CAD/CAM del mismo modo que la barra anteriormente descrita, con la diferencia de que sobre ellas se colocó un recubrimiento de cerámica (figs. 47-49). La paciente continúa en seguimiento, sin evidenciarse pérdidas óseas significativas en ninguno de los implantes estrechos y cortos que conforman la restauración de todo el maxilar superior tras tres años de carga de la prótesis definitiva (y hasta 4,5 de la carga de los implantes de la fase inicial de carga inmediata) (fig. 50).
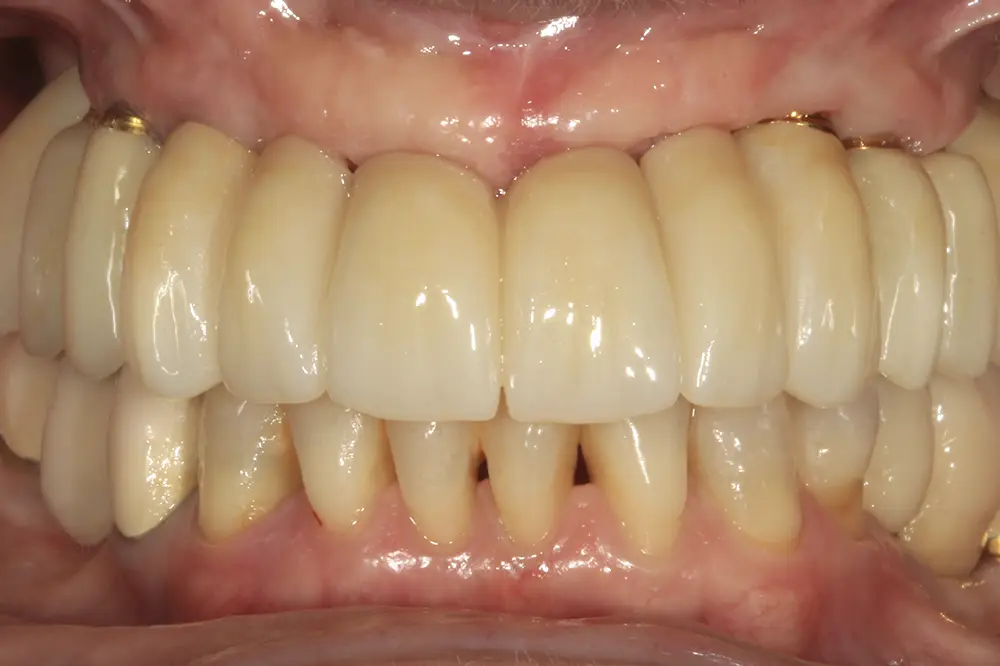
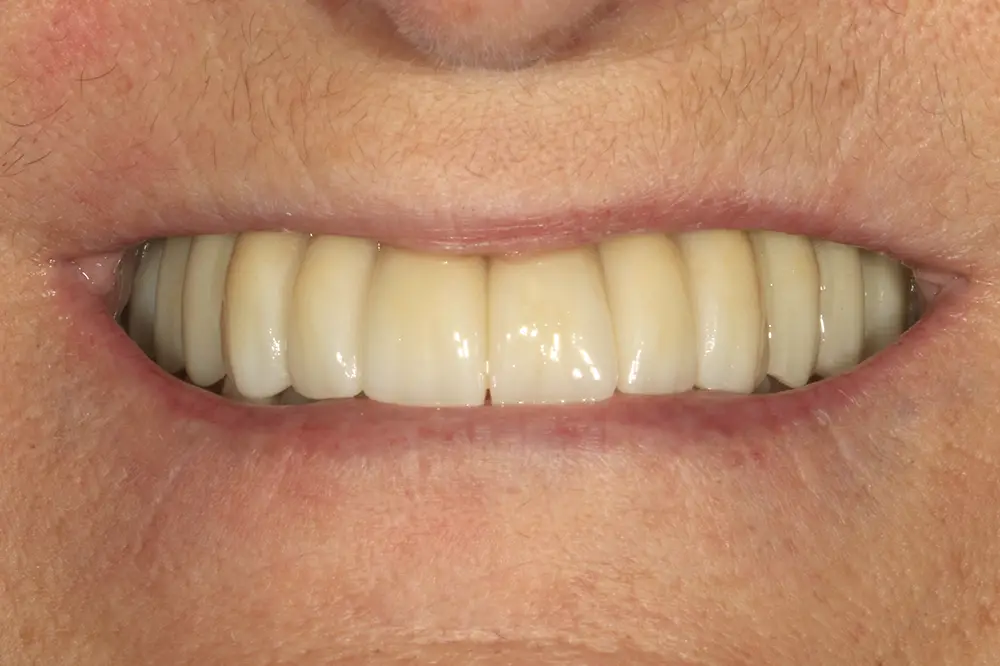
Figs. 47 y 48. Prótesis terminadas, colocadas en la paciente.
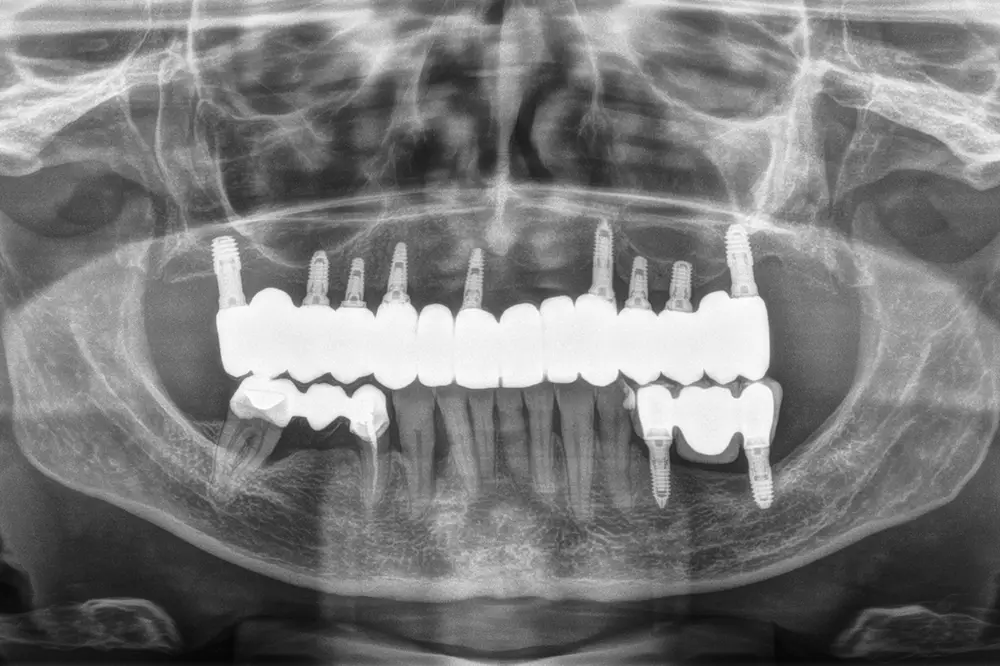
Fig. 49. Radiografía final en el momento de colocación de la prótesis, dividida en los tres sectores.
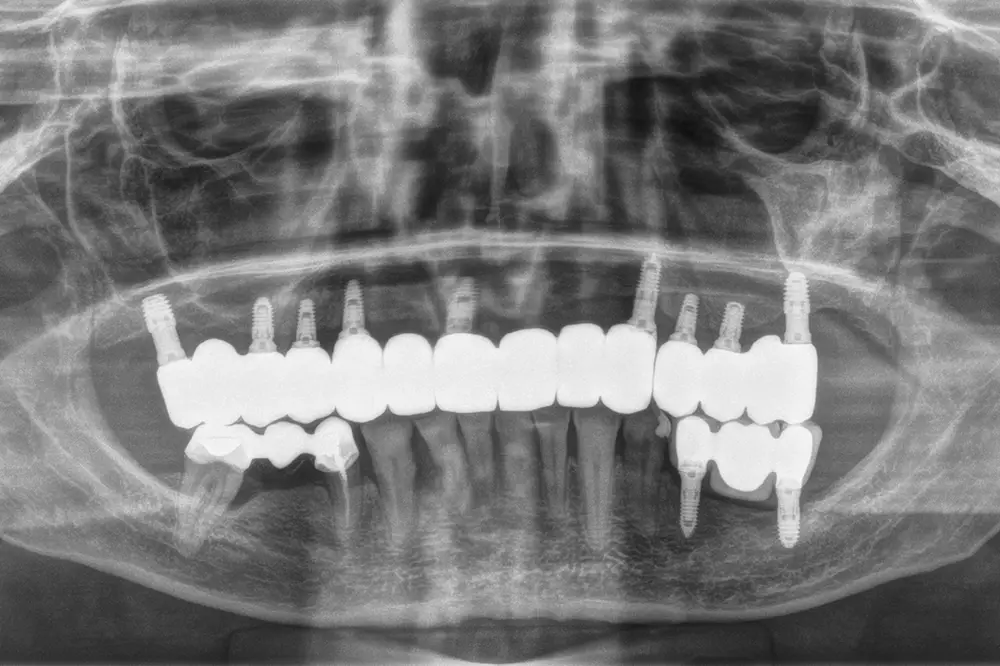
Fig. 50. Imagen radiográfica de la paciente a los 3 años de la carga definitiva y 4,5 años tras la carga inicial de los implantes colocados inicialmente para la carga inmediata. En ella vemos la estabilidad del tratamiento en el tiempo de seguimiento ofrecido.
Discusión
La rehabilitación del maxilar superior con atrofia extrema continúa siendo uno de los mayores retos en implantología oral, especialmente cuando coexisten déficits combinados de volumen óseo en sentido vertical y horizontal. Tradicionalmente, estos casos requerían procedimientos reconstructivos complejos, como injertos en bloque, elevaciones sinusal laterales o regeneraciones guiadas de gran volumen, acompañados habitualmente de una elevada morbilidad, tiempos prolongados de tratamiento y una mayor probabilidad de complicaciones postquirúrgicas10,11,48,50–52,52–54. En este contexto, el desarrollo y validación clínica de los implantes estrechos, cortos y extracortos ha permitido plantear alternativas menos invasivas y, en muchos casos, igualmente predecibles, incluso en escenarios anatómicos altamente limitados5,19,40,42,43,55–60.
Los resultados de diversas revisiones sistemáticas han demostrado que tanto los implantes de diámetro reducido como los implantes de longitud corta pueden alcanzar tasas de supervivencia comparables a las de los implantes convencionales, siempre que exista un protocolo quirúrgico adecuado, una selección cuidadosa del caso y una distribución biomecánica favorable10,22,28,34,39,43,58,59,61–64. Esta evidencia ha impulsado un cambio progresivo hacia enfoques terapéuticos más conservadores, que priorizan la preservación del hueso remanente, disminuyen la necesidad de cirugía reconstructiva y reducen la agresividad global del tratamiento5,19,24,27. En atrofias severas, esta filosofía resulta especialmente relevante, dado que el hueso disponible suele ser limitado y debe ser preservado para mantener la predictibilidad funcional a largo plazo25,27,35,65.
El caso presentado ilustra de manera clara cómo la combinación estratégica de implantes estrechos y cortos con técnicas quirúrgicas mínimamente invasivas como las que hemos presentado: como la expansión de cresta, la elevación transcrestal con fresa de ataque frontal o el empleo de biomateriales autólogos y PRGF-Endoret, permite rehabilitar un maxilar extremadamente atrófico sin recurrir a procedimientos reconstructivos mayores16,25,26,29,37,46,55,66. Las decisiones terapéuticas estuvieron guiadas por una planificación tridimensional exhaustiva, basada en CBCT y en el análisis morfológico individualizado de cada segmento del maxilar, lo que permitió adaptar el diámetro, la longitud y el protocolo de fresado de cada implante a las condiciones específicas del lecho receptor46. Este planteamiento quirúrgico integral, apoyado en la evidencia actual, demuestra que es posible optimizar el volumen óseo disponible y lograr una inserción segura incluso en crestas con alturas inferiores a 4 mm o anchuras de apenas 3 mm16,25,26,55,66,67.
Asimismo, la secuencia protésica realizada, basada en una estrategia de carga progresiva y en la utilización de estructuras CAD/CAM en titanio, incluyendo la barra Blender en el sector anterior, contribuyó de forma determinante a la estabilidad biomecánica del conjunto68. El diseño monolítico fresado en titanio proporciona un ajuste pasivo altamente preciso, indispensable en rehabilitaciones implantosoportadas en zonas estéticas, más aún con implantes cortos y estrechos, donde la distribución de cargas y la estabilidad a largo plazo resultan críticas. Además, la combinación de esta estructura con un recubrimiento cerámico de circonio permite obtener una elevada resistencia mecánica junto con una óptima integración estética, ofreciendo una transición más natural con los tejidos periimplantarios y una mejor mimetización cromática en comparación con otros materiales68–70. Esta configuración reduce el riesgo de fracturas cerámicas, minimiza tensiones sobre los implantes y facilita el mantenimiento del paciente, por lo que se consideró la alternativa más adecuada para garantizar durabilidad, funcionalidad y un resultado estético de alta calidad en el sector anterior70. Además, la posibilidad de unir progresivamente los implantes conforme se completaban las fases quirúrgicas permitió no solo mantener una función adecuada durante todo el tratamiento, sino también garantizar una distribución homogénea de cargas, reduciendo el riesgo de micromovimientos adversos en los periodos críticos de osteointegración. Este enfoque es por lo tanto coherente con los principios de la implantología moderna, que abogan por la minimización de fases quirúrgicas y protésicas sin comprometer la estabilidad biomecánica y los resultados a largo plazo.
Bibliografía
- Gaviria L, Salcido JP, Guda T, Ong JL. Current trends in dental implants. J Korean Assoc Oral Maxillofac Surg. 2014;40: 50–60. doi:10.5125/jkaoms.2014.40.2.50
- Jung RE, Al-Nawas B, Araujo M, Avila-Ortiz G, Barter S, Brodala N, et al. Group 1 ITI Consensus Report: The influence of implant length and design and medications on clinical and patient-reported outcomes. Clin Oral Implants Res. 2018;29: 69–77. doi:10.1111/clr.13342
- Romeo E, Storelli S. Systematic review of the survival rate and the biological, technical, and aesthetic complications of fixed dental prostheses with cantilevers on implants reported in longitudinal studies with a mean of 5 years follow-up. Clin Oral Implants Res. 2012;23: 39–49. doi:10.1111/J.1600-0501.2012.02551.X
- Anitua E, Flores C, Piñas L, Alkhraisat MH. Frequency of technical complications in fixed implant prosthesis: The effect of prosthesis screw emergence correction by computer-aided design/computer-aided manufacturing. Journal of Oral Implantology. 2018;44: 427–431. doi:10.1563/AAID-JOI-D-17-00229
- Nisand D, Renouard F. Short implant in limited bone volume. Periodontol 2000. 2014;66: 72–96. doi:10.1111/prd.12053
- Yu X, Xu R, Zhang Z, Yang Y, Deng F. A meta-analysis indicating extra-short implants (≤ 6 mm) as an alternative to longer implants (≥ 8 mm) with bone augmentation. Scientific Reports 2021 11:1. 2021;11: 8152-. doi:10.1038/s41598-021-87507-1
- Torres-Alemany A, Fernández-Estevan L, Agustín-Panadero R, Montiel-Company JM, Labaig-Rueda C, Mañes-Ferrer JF. Clinical Behavior of Short Dental Implants: Systematic Review and Meta-Analysis. Journal of Clinical Medicine 2020, Vol 9, Page 3271. 2020;9: 3271. doi:10.3390/JCM9103271
- Pieri F, Forlivesi C, Caselli E, Corinaldesi G. Narrow‐ (3.0 mm) Versus Standard‐Diameter (4.0 and 4.5 mm) Implants for Splinted Partial Fixed Restoration of Posterior Mandibular and Maxillary Jaws: A 5‐Year Retrospective Cohort Study. J Periodontol. 2017;88: 338–347. doi:10.1902/jop.2016.160510
- Anitua E, Murias-Freijo A, Alkhraisat MH, Orive G. Implant-Guided vertical bone augmentation around extra-short implants for the management of severe bone atrophy. Journal of Oral Implantology. 2015;41: 563–569. doi:10.1563/AAID-JOI-D-13-00131
- Elnayef B, Monje A, Lin G-H, Gargallo-Albiol J, Chan H-L, Wang H-L, et al. Alveolar Ridge Split on Horizontal Bone Augmentation: A Systematic Review. Int J Oral Maxillofac Implants. 2015;30: 596–606. doi:10.11607/JOMI.4051
- Mertens C, Freier K, Engel M, Krisam J, Hoffmann J, Freudlsperger C. Reconstruction of the severely atrophic edentulous maxillae with calvarial bone grafts. Clin Oral Implants Res. 2017;28: 749–756. doi:10.1111/CLR.12873
- Van Der Weijden F, Dell’Acqua F, Slot DE. Alveolar bone dimensional changes of post-extraction sockets in humans: A systematic review. J Clin Periodontol. 2009;36: 1048–1058. doi:10.1111/J.1600-051X.2009.01482.X
- Toledano-Osorio M, Toledano M, Manzano-Moreno FJ, Vallecillo C, Vallecillo-Rivas M, Rodriguez-Archilla A, et al. Alveolar bone ridge augmentation using polymeric membranes: A systematic review and meta-analysis. Polymers (Basel). 2021;13. doi:10.3390/POLYM13071172
- Milinkovic I, Cordaro L. Are there specific indications for the different alveolar bone augmentation procedures for implant placement? A systematic review. Int J Oral Maxillofac Surg. 2014;43: 606–625. doi:10.1016/J.IJOM.2013.12.004
- Roccuzzo A, Marchese S, Worsaae N, Jensen SS. The sandwich osteotomy technique to treat vertical alveolar bone defects prior to implant placement: a systematic review. Clin Oral Investig. 2020;24: 1073–1089. doi:10.1007/S00784-019-03183-6
- Anitua E, Flores J, Alkhraisat MH. Transcrestal Sinus Lift Using Platelet Concentrates in Association to Short Implant Placement: A Retrospective Study of Augmented Bone Height Remodeling. Clin Implant Dent Relat Res. 2016;18: 993–1002. doi:10.1111/CID.12383
- Camps‐Font O, Burgueño‐Barris G, Figueiredo R, Jung RE, Gay‐Escoda C, Valmaseda‐Castellón E. Interventions for Dental Implant Placement in Atrophic Edentulous Mandibles: Vertical Bone Augmentation and Alternative Treatments. A Meta‐Analysis of Randomized Clinical Trials. J Periodontol. 2016;87: 1444–1457. doi:10.1902/JOP.2016.160226
- Antiua E, Escuer V, Alkhraisat MH. Short Narrow Dental Implants versus Long Narrow Dental Implants in Fixed Prostheses: A Prospective Clinical Study. Dent J (Basel). 2022;10: 39. doi:10.3390/DJ10030039
- Antiua E, Escuer V, Alkhraisat MH. Short Narrow Dental Implants versus Long Narrow Dental Implants in Fixed Prostheses: A Prospective Clinical Study. Dent J (Basel). 2022;10: 39. doi:10.3390/DJ10030039
- Short Narrow Dental Implants versus Long Narrow Dental Implants in Fixed Prostheses: A Prospective Clinical Study – PMC. [cited 19 Nov 2025]. Available: https://pmc.ncbi.nlm.nih.gov/articles/PMC8947067/?utm_source=chatgpt.com
- Maló PS, de Araújo Nobre MA, Lopes A V., Ferro AS. Retrospective cohort clinical investigation of a dental implant with a narrow diameter and short length for the partial rehabilitation of extremely atrophic jaws. J Oral Sci. 2017;59: 357–363. doi:10.2334/JOSNUSD.16-0321
- Klein M, Schiegnitz E, Al-Nawas B. Systematic Review on Success of Narrow-Diameter Dental Implants. Int J Oral Maxillofac Implants. 2014;29: 43–54. doi:10.11607/JOMI.2014SUPPL.G1.3
- Schiegnitz E, Al-Nawas B. Narrow-diameter implants: A systematic review and meta-analysis. Clin Oral Implants Res. 2018;29: 21–40. doi:10.1111/CLR.13272
- Ramani S, Vijayalakshmi R, Kumari CBN, Mahendra J, Ambalavanan N. A short review on minimally invasive implants. Bioinformation. 2023;19: 655. doi:10.6026/97320630019655
- Anitua E, Fernandez-de-Retana S, Anitua B, Alkhraisat M. Long-Term Retrospective Study of 3.0-mm-Diameter Implants Supporting Fixed Multiple Prostheses: Immediate Versus Delayed Implant Loading. Int J Oral Maxillofac Implants. 2020;35: 1229–1238. doi:10.11607/JOMI.8180
- Anitua E, Alkhraisat MH. Single-unit short dental implants. Would they survive a long period of service? British Journal of Oral and Maxillofacial Surgery. 2019;57: 387–388. doi:10.1016/J.BJOMS.2019.03.005
- Anitua E. [Rehabilitation of a case with active periodontitis and advanced perii-implantitis. Minimally invasive approach]. Revista cientifica odontologica (Universidad Cientifica del Sur). 2022;10: e113. doi:10.21142/2523-2754-1002-2022-113
- Assaf A, Saad M, Daas M, Abdallah J, Abdallah R. Use of narrow-diameter implants in the posterior jaw: A systematic review. Implant Dent. 2015;24: 294–306. doi:10.1097/ID.0000000000000238
- Anitua E, Saracho J, Begoña L, Alkhraisat MH. Long-Term Follow-Up of 2.5-mm Narrow-Diameter Implants Supporting a Fixed Prostheses. Clin Implant Dent Relat Res. 2016;18: 769–777. doi:10.1111/CID.12350
- Mangano F, Shibli JA, Sammons RL, Veronesi G, Piattelli A, Mangano C. Clinical Outcome of Narrow-Diameter (3.3-mm) Locking-Taper Implants: A Prospective Study with 1 to 10 Years of Follow-up. Int J Oral Maxillofac Implants. 2014;29: 448–455. doi:10.11607/JOMI.3327
- Pieri F, Forlivesi C, Caselli E, Corinaldesi G. Narrow‐ (3.0 mm) Versus Standard‐Diameter (4.0 and 4.5 mm) Implants for Splinted Partial Fixed Restoration of Posterior Mandibular and Maxillary Jaws: A 5‐Year Retrospective Cohort Study. J Periodontol. 2017;88: 338–347. doi:10.1902/JOP.2016.160510
- Ma M, Qi M, Zhang D, Liu H. The Clinical Performance of Narrow Diameter Implants Versus Regular Diameter Implants: A Meta-Analysis. Journal of Oral Implantology. 2019;45: 503–508. doi:10.1563/AAID-JOI-D-19-00025
- Arsan V, Bölükbaş N, Ersanli S, Özdemir T. Evaluation of 316 narrow diameter implants followed for 5-10 years: A clinical and radiographic retrospective study. Clin Oral Implants Res. 2010;21: 296–307. doi:10.1111/J.1600-0501.2009.01840.X
- Alrabiah M. Comparison of survival rate and crestal bone loss of narrow diameter dental implants versus regular dental implants: A systematic review and meta-analysis. J Investig Clin Dent. 2019;10: e12367. doi:10.1111/JICD.12367
- Anitua E, Orive G. A new approach for atraumatic implant explantation and immediate implant installation. Oral Surg Oral Med Oral Pathol Oral Radiol. 2012;113. doi:10.1016/j.tripleo.2011.06.035
- Anitua E, Alkhraisat MH. Is Alveolar Ridge Split a Risk Factor for Implant Survival? Journal of Oral and Maxillofacial Surgery. 2016;74: 2182–2191. doi:10.1016/J.JOMS.2016.06.182
- Anitua E, Prado R, Orive G, Tejero R. Effects of calcium-modified titanium implant surfaces on platelet activation, clot formation, and osseointegration. J Biomed Mater Res A. 2015;103: 969–980. doi:10.1002/JBM.A.35240
- Anitua E, Larrazabal Saez de Ibarra N, Morales Martín I, Saracho Rotaeche L. Influence of dental implant diameter and bone quality on the biomechanics of single-crown restoration. A finite element analysis. Dent J (Basel). 2021;9. doi:10.3390/DJ9090103
- Ravidà A, Wang IC, Sammartino G, Barootchi S, Tattan M, Troiano G, et al. Prosthetic Rehabilitation of the Posterior Atrophic Maxilla, Short (≤6 mm) or Long (≥10 mm) Dental Implants? A Systematic Review, Meta-analysis, and Trial Sequential Analysis: Naples Consensus Report Working Group A. Implant Dent. 2019;28: 590–602. doi:10.1097/ID.0000000000000919
- Anitua E, Flores J, Flores C, Alkhraisat M. Long-term Outcomes of Immediate Loading of Short Implants: A Controlled Retrospective Cohort Study. Int J Oral Maxillofac Implants. 2016;31: 1360–1366. doi:10.11607/JOMI.5330
- Cruz RS, de Araújo Lemos CA, de Souza Batista VE, e Oliveira HFF, de Luna Gomes JM, Pellizzer EP, et al. Short implants versus longer implants with maxillary sinus lift. A systematic review and meta-analysis. Braz Oral Res. 2018;32: 1–14. doi:10.1590/1807-3107BOR-2018.VOL32.0086
- Lozano-Carrascal N, Anglada-Bosqued A, Salomó-Coll O, Hernández-Alfaro F, Wang HL, Gargallo-Albiol J. Short implants (<8mm) versus longer implants (≥8mm) with lateral sinus floor augmentation in posterior atrophic maxilla: A meta-analysis of RCT`s in humans. Med Oral Patol Oral Cir Bucal. 2020;25: e168–e179. doi:10.4317/MEDORAL.23248
- Altaib FH, Alqutaibi AY, Al-Fahd A, Eid S. Short dental implant as alternative to long implant with bone augmentation of the atrophic posterior ridge: A systematic review and meta-analysis of RCTs. Quintessence Int (Berl). 2019. doi:10.3290/J.QI.A42948
- Anitua E, Piñas L, Alkhraisat MH. A Novel Technique for Preparation of Recipient Site and Autologous Bone Grafting in Autotransplantation of Single-Rooted Teeth: A Report of Two Cases. Cureus. 2022;14: e31888. doi:10.7759/cureus.31888
- Anitua E, Carda C, Andia I. A novel drilling procedure and subsequent bone autograft preparation: a technical note. Int J Oral Maxillofac Implants. 22: 138–45. Available: http://www.ncbi.nlm.nih.gov/pubmed/17340908
- Anitua E, Alkhraisat MH, Piñas L, Orive G. Efficacy of biologically guided implant site preparation to obtain adequate primary implant stability. Annals of Anatomy. 2015;199: 9–15. doi:10.1016/j.aanat.2014.02.005
- Anitua E, Flores C, Fernández-de-Retana S, Anitua B, Alkhraisat MH. Performance of Immediately Loaded Short Implants Using Low-Speed Drilling Protocol and Plasma Rich in Growth Factors: A Controlled Retrospective Observational Study. International Journal of Periodontics and Restorative Dentistry. 2023;43: 232–239b. doi:10.11607/prd.5203
- Anitua E, Begoña L, Orive G. Controlled ridge expansion using a two-stage split-crest technique with ultrasonic bone surgery. Implant Dent. 2012;21: 163–170. doi:10.1097/ID.0b013e318249f50b
- Anitua E, Begoña L, Orive G. Clinical evaluation of split-crest technique with ultrasonic bone surgery for narrow ridge expansion: Status of soft and hard tissues and implant success. Clin Implant Dent Relat Res. 2013;15: 176–187. doi:10.1111/j.1708-8208.2011.00340.x
- Urban IA, Monje A. Guided Bone Regeneration in Alveolar Bone Reconstruction. Oral Maxillofac Surg Clin North Am. 2019;31: 331–338. doi:10.1016/j.coms.2019.01.003
- Jepsen S, Schwarz F, Cordaro L, Derks J, Hämmerle CHF, Heitz-Mayfield LJ, et al. Regeneration of alveolar ridge defects. Consensus report of group 4 of the 15th European Workshop on Periodontology on Bone Regeneration. J Clin Periodontol. 2019;46: 277–286. doi:10.1111/jcpe.13121
- Urban IA, Monje A, Lozada JL, Wang HL. Long-term Evaluation of Peri-implant Bone Level after Reconstruction of Severely Atrophic Edentulous Maxilla via Vertical and Horizontal Guided Bone Regeneration in Combination with Sinus Augmentation: A Case Series with 1 to 15 Years of Loading. Clin Implant Dent Relat Res. 2017;19: 46–55. doi:10.1111/CID.12431
- McAllister BS, Haghighat K. Bone Augmentation Techniques. J Periodontol. 2007;78: 377–396. doi:10.1902/jop.2007.060048
- Roccuzzo A, Imber JC, Jensen SS. Need for lateral bone augmentation at two narrow-diameter implants: A prospective, controlled, clinical study. Clin Oral Implants Res. 2021;32: 511–520. doi:10.1111/CLR.13721
- Anitua E, Alkhraisat MH. 15-year follow-up of short dental implants placed in the partially edentulous patient: Mandible Vs maxilla. Annals of Anatomy. 2019;222: 88–93. doi:10.1016/J.AANAT.2018.11.003
- Anitua E, Alkhraisat MH. Fifteen-Year Follow-up of Short Dental Implants in the Completely Edentulous Jaw: Submerged Versus Nonsubmerged Healing. Implant Dent. 2019;28: 551–555. doi:10.1097/ID.0000000000000935
- Chen S, Ou Q, Wang Y, Lin X. Short implants (5-8 mm) vs long implants (≥10 mm) with augmentation in atrophic posterior jaws: A meta-analysis of randomised controlled trials. J Oral Rehabil. 2019;46: 1192–1203. doi:10.1111/JOOR.12860
- de FJ, Pecorari VGA, Martins CB, Del Fabbro M, Casati MZ. Short implants versus bone augmentation in combination with standard-length implants in posterior atrophic partially edentulous mandibles: systematic review and meta-analysis with the Bayesian approach. Int J Oral Maxillofac Surg. 2019;48: 90–96. doi:10.1016/J.IJOM.2018.05.009
- Al-Johany S. Survival Rates of Short Dental Implants (≤ 6.5 mm) Placed in Posterior Edentulous Ridges and Factors Affecting Their Survival After a 12-Month Follow-up Period: Systematic Review. Int J Oral Maxillofac Implants. 2019;34: 605–621. doi:10.11607/jomi.7187
- Anitua E, Alkhraist M, Piñas L, Begoña L, Orive G. Implant Survival and Crestal Bone Loss Around Extra-Short Implants Supporting a Fixed Denture: The Effect of Crown Height Space, Crown-to-Implant Ratio, and Offset Placement of the Prosthesis. Int J Oral Maxillofac Implants. 2014;29: 682–689. doi:10.11607/JOMI.3404
- Schiegnitz E, Al-Nawas B. Narrow-diameter implants: A systematic review and meta-analysis. Clin Oral Implants Res. 2018;29 Suppl 16: 21–40. doi:10.1111/CLR.13272
- Pesce P, Del Fabbro M, Modenese L, Sandron S, Francetti L, Isola G, et al. Influence of implant diameter on implant survival rate and clinical outcomes in the posterior area: a systematic review and meta-analysis. BMC Oral Health. 2023;23: 235-. doi:10.1186/S12903-023-02962-8/FIGURES/6
- Alrabiah M. Comparison of survival rate and crestal bone loss of narrow diameter dental implants versus regular dental implants: A systematic review and meta-analysis. J Investig Clin Dent. 2019;10: e12367. doi:10.1111/jicd.12367
- Aglietta M, Siciliano VI, Zwahlen M, Brägger U, Pjetursson BE, Lang NP, et al. A systematic review of the survival and complication rates of implant supported fixed dental prostheses with cantilever extensions after an observation period of at least 5 years. Clin Oral Implants Res. 2009;20: 441–451. doi:10.1111/J.1600-0501.2009.01706.X
- Anitua E, Hamdan Alkhraisat M, Orive G. Novel Technique for the Treatment of the Severely Atrophied Posterior Mandible. Int J Oral Maxillofac Implants. 2013;28: 1338–1346. doi:10.11607/JOMI.3137
- Anitua E, Fernandez-de-Retana S, Anitua B, Alkhraisat M. Long-Term Retrospective Study of 3.0-mm-Diameter Implants Supporting Fixed Multiple Prostheses: Immediate Versus Delayed Implant Loading. Int J Oral Maxillofac Implants. 2020;35: 1229–1238. doi:10.11607/jomi.8180
- Anitua E, Padilla S, Alkhraisat MH. Transalveolar Osteotomy of the Mandibular Canal Wall for the Treatment of Severely Atrophied Posterior Mandible. Journal of Oral and Maxillofacial Surgery. 2017;75: 1392–1401. doi:10.1016/J.JOMS.2017.03.004
- Watanabe H, Fellows C, An H. Digital Technologies for Restorative Dentistry. Dent Clin North Am. 2022;66: 567–590. doi:10.1016/j.cden.2022.05.006
- Parpaiola A, Toia M, Norton M, Rodriguez Y Baena R, Todaro C, Lupi SM. Fully digital workflow for implant-supported fixed restorations consisting of a titanium primary structure and a zirconia secondary structure. Int J Oral Implantol (Berl). 2023;16: 351–358. Available: http://www.ncbi.nlm.nih.gov/pubmed/37994822
- Mijiritsky E, Elad A, Krausz R, Ivanova V, Zlatev S. Clinical performance of full-arch implant-supported fixed restorations made of monolithic zirconia luted to a titanium bar: A retrospective study with a mean follow-up of 16 months. J Dent. 2023;137. doi:10.1016/j.jdent.2023.104675
Suscríbete a nuestra Newsletter
Mantente al día de las últimas novedades del mundo dental
Información legal
Reponsable: rIL Estudio, S.L.
Finalidad: Consentimiento expreso del interesado (Art. 6.1.a RGPD).
Destinatarios: Los datos no se cederán a terceros, salvo obligación legal o los proveedores de servicios de email marketing que actúan como encargados del tratamiento (ej. Mailrelay, Mailchimp, Brevo, etc.) bajo acuerdos de confidencialidad.
Derechos: Acceder, rectificar y suprimir los datos, así como otros derechos, como se explica en la información adicional.
Información Adicional: Puedes consultar la información detallada en nuestra Política de Privacidad.