El estudio, dirigido por el biólogo oral Jorge Frías-López, se centró en P. gingivalis, considerada por la comunidad científica como un “patógeno clave” en el desarrollo de la periodontitis. Aunque puede encontrarse en cantidades relativamente pequeñas, esta bacteria tiene la capacidad de alterar el equilibrio de toda la comunidad microbiana de la cavidad oral, favoreciendo la aparición de inflamación y destrucción de los tejidos de soporte del diente.
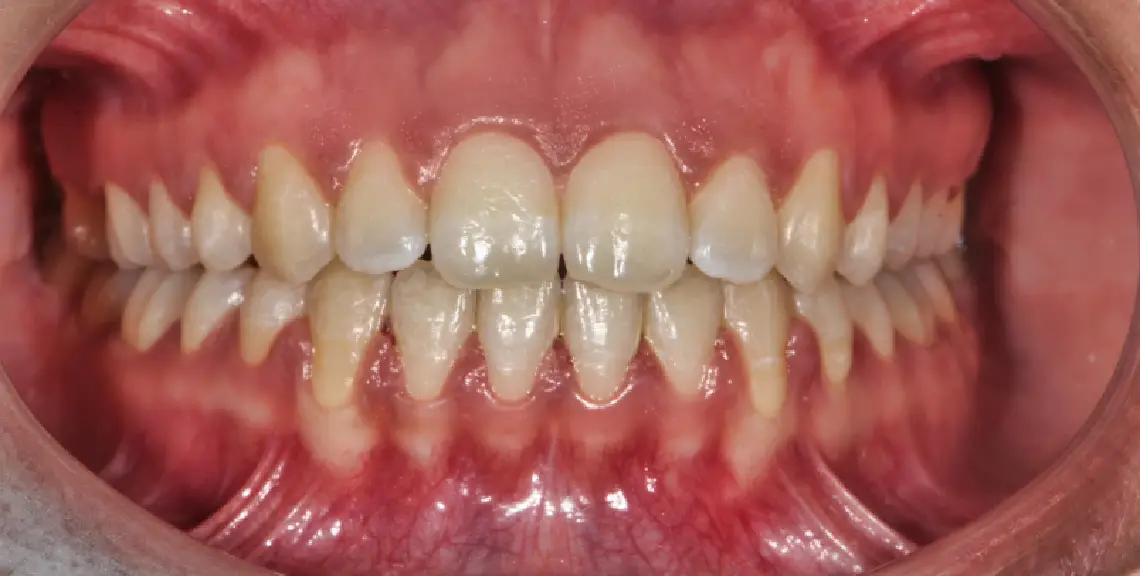
La enfermedad periodontal sigue representando un importante problema de salud pública. En Estados Unidos, se estima que afecta a aproximadamente el 42 % de los adultos mayores de 30 años y constituye una de las principales causas de pérdida dentaria debido a la destrucción progresiva del hueso alveolar.
En la práctica clínica, el tratamiento de la periodontitis se basa principalmente en la eliminación mecánica de la placa y el cálculo subgingival mediante raspado y alisado radicular, así como en el uso de antibióticos o procedimientos quirúrgicos en casos avanzados. Aunque estas estrategias resultan eficaces para reducir la carga bacteriana, también pueden afectar de forma indiscriminada a bacterias beneficiosas del microbioma oral. Con el objetivo de encontrar enfoques terapéuticos más específicos, el equipo investigador analizó el sistema CRISPR de P. gingivalis. Aunque esta tecnología es conocida actualmente por su uso en edición genética, originalmente forma parte del sistema inmunitario de las bacterias, que lo utilizan para defenderse de virus.
Durante el estudio, los científicos se centraron en una región particular del genoma bacteriano, denominada anteriormente matriz CRISPR 30.1. A diferencia de otros sistemas CRISPR, cuyos fragmentos genéticos suelen corresponder a virus invasores, esta secuencia contenía fragmentos de ADN que coincidían con el propio genoma de la bacteria.
Para comprender su función, los investigadores eliminaron experimentalmente esta matriz genética. El resultado fue inesperado: lejos de debilitar a la bacteria, su eliminación la volvió significativamente más agresiva. La cepa modificada produjo aproximadamente el doble de biopelícula —la estructura bacteriana que forma la placa dental— y generó una respuesta inflamatoria mucho más intensa en células inmunitarias humanas.
Estos resultados sugieren que la matriz CRISPR 30.1 actúa como un “freno genético” que limita la agresividad de P. gingivalis. Según los investigadores, este mecanismo permitiría al patógeno mantener un nivel de actividad suficiente para persistir en el tejido gingival sin desencadenar una respuesta inmunitaria masiva que lo elimine rápidamente, favoreciendo así infecciones crónicas.
A partir de este hallazgo, los científicos plantean la posibilidad de desarrollar terapias dirigidas específicamente contra este patógeno. Una de las estrategias propuestas consistiría en utilizar bacteriófagos —virus que infectan bacterias— modificados para reconocer P. gingivalis e introducir instrucciones genéticas que alteren este sistema regulador. Este enfoque permitiría controlar la actividad de la bacteria sin eliminar otras especies beneficiosas del microbioma oral, lo que representaría un cambio significativo respecto a los tratamientos actuales.
Los investigadores señalan además que las implicaciones del estudio podrían ir más allá de la salud bucodental. Numerosas investigaciones han relacionado la periodontitis con enfermedades sistémicas como las patologías cardiovasculares o la diabetes, en parte debido a la entrada de toxinas bacterianas en el torrente sanguíneo desde los tejidos gingivales inflamados.
Controlar de forma más precisa la actividad de P. gingivalis podría, por tanto, contribuir no solo a preservar los tejidos periodontales y prevenir la pérdida dental, sino también a reducir procesos inflamatorios sistémicos asociados a la enfermedad periodontal.